| Numéro |
Biologie Aujourd’hui
Volume 217, Numéro 3-4, 2023
|
|
|---|---|---|
| Page(s) | 253 - 263 | |
| DOI | https://doi.org/10.1051/jbio/2023031 | |
| Publié en ligne | 29 novembre 2023 | |
Article
Intérêt du régime cétogène dans la prise en charge de la maladie d’Alzheimer
Beneficial effects of ketogenic diet for Alzheimer’s disease management
Université de Strasbourg, CRBS, UR3072 « Mitochondrie, stress oxydant et protection musculaire », 1 rue Eugène Boeckel, 67000 Strasbourg, France
* Auteurs correspondants: Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
; Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
.
Reçu :
21
Août
2023
Résumé
La maladie d’Alzheimer (MA), pathologie neurodégénérative en expansion, devient une préoccupation importante de santé publique, en raison d’une absence de traitement curatif efficace. Les mécanismes mis en œuvre dans la physiopathologie de la MA sont de mieux en mieux connus, et incluent l’accumulation de plaques amyloïdes et de dégénérescences neurofibrillaires. L’augmentation de l’inflammation et du stress oxydant et l’altération du métabolisme cérébral du glucose aggravent la pathologie en réduisant l’activité neuronale en perturbant la fonction mitochondriale. À l’heure actuelle, le traitement de cette pathologie regroupe différentes approches bien que ces interventions n’aient pas un effet curatif, mais uniquement compensatoire. L’alimentation cétogène, pauvre en glucides et enrichie en lipides, couplée à une prise de triglycérides à chaîne moyenne (MCT), favorise la production de corps cétoniques, substrats énergétiques qui pourraient présenter des effets neuroprotecteurs bénéfiques pour les personnes atteintes de la MA. Une telle prise en charge nutritionnelle pourrait limiter la progression de la maladie et améliorer les capacités cognitives des patients. Cette revue vise à examiner le rôle éventuel et les mécanismes neuroprotecteurs de l’alimentation cétogène dans la progression de la MA, et décrit les avantages et les limites de son utilisation comme stratégie thérapeutique.
Abstract
Alzheimer’s disease (AD) is a neurodegenerative disease that affects almost 1 million people in France and 55 million in the world. This pathology is a global health preoccupation because of the lack of efficient curative treatment and the increase of its prevalence. During the last decade, the comprehension of pathophysiological mechanisms involved in AD have been improved. Amyloid plaques and neurofibrillary tangles accumulation are characteristic of Alzheimer’s brain patients, accompanied by increased brain inflammation and oxidative stress, impaired cerebral metabolism of glucose and mitochondrial function. Treatment of AD includes different approaches, as pharmacology, psychology support, physiotherapy, and speech therapy. However, these interventions do not have a curative effect, but only compensatory on the disease. Ketogenic diet (KD), a low-carbohydrates and high-fat diet, associated with a medium-chain triglycerides intake (MCTs) might induce benefices for Alzheimer disease patients. Carbohydrate restriction and MCTs promotes the production of ketone bodies from fatty acid degradation. These metabolites replacing glucose, serve the brain as energetic substrates, and induce neuroprotective effects. Such a nutritional support might slow down the disease progression and improve cognitive abilities of patients. This review aims to examine the neuroprotective mechanisms of KD in AD progression and describes the advantages and limitations of KD as a therapeutic strategy.
Mots clés : maladie d’Alzheimer / régime cétogène / triglycérides à chaîne moyenne / corps cétoniques / glucose
Key words: Alzheimer’s disease / ketogenic diet / medium chain triglycerides / ketone bodies / glucose
© Société de Biologie, 2023
Abréviations
ATP : Adénosine tri-phosphate
BHB : β-hydroxybutyrate
FADH2 : Flavine adénine dinucléotide
KD : Régime cétogène (Ketogenic Diet)
MA : Maladie d’Alzheimer
MCT : Acides gras à chaîne moyenne (Medium Chain Triglycerides)
NADH : H+ (Nicotinamide adénine dinucléotide)
PET : Émission de positons
Présentation de la physiopathologie de la maladie d’Alzheimer
Épidémiologie et signes cliniques de la maladie d’Alzheimer
La maladie d’Alzheimer (MA) est la plus fréquente des maladies neurodégénératives touchant les personnes âgées. Selon les données de l’Organisation Mondiale de la Santé, elle est à l’origine de 60 % à 70 % des démences parmi les 55 millions de personnes atteintes de démences dans le monde. Les prévisions estiment qu’en 2050, ces chiffres auront triplé pour toucher 152 millions de personnes (Organisation Mondiale de la Santé, 2020). Les taux de prévalence de la MA sont de 10 % après 65 ans et augmentent à 40 % après 85 ans (Kumar et al., 2021). Il s’agit donc d’une préoccupation majeure de santé publique.
La MA est une démence qui s’installe de manière lente et progressive avec des troubles insidieux, car lorsque les premiers symptômes sont détectés, la maladie est déjà en place depuis une dizaine d’années (Soria Lopez et al., 2019). La dégénérescence peut se découper en plusieurs stades, où les symptômes s’aggravent progressivement (Figure 1). En premier, le stade préclinique (qui se développe sur une durée de 10 à 20 ans) où il n’y a pas de signe clinique visible, puis le stade pré-démentiel (5 ans), le stade démentiel (3 à 10 ans) et enfin le stade démentiel évolué (Jack et al., 2018).
 |
Figure 1 Stades d’évolution de la maladie d’Alzheimer. La maladie d’Alzheimer est progressive et se développe selon 4 stades : préclinique, prédémentiel, démentiel et démentiel évolué, où les symptômes de la maladie s’aggravent progressivement, jusqu’au décès du patient. |
Facteurs de risques impliqués dans le développement de la maladie d’Alzheimer
La MA est une maladie multifactorielle, causée par des facteurs génétiques et environnementaux (INSERM, 2006). Quatre gènes sont impliqués dans les très rares formes monogéniques de MA, le plus fréquemment concerné étant le gène encodant la préséniline 1 (PSEN1) Ces mutations génétiques ont pour conséquence la production du peptide amyloïde (Aβ), dont l’accumulation sous forme de plaques est un des deux signes pathognomiques de la MA (Soria Lopez et al., 2019). Il existe aussi de nombreux facteurs de risque génétique des formes sporadiques, en particulier l’allèle ApoE4 de l’apolipoprotéine E (Zhong & Weisgraber, 2009).
Les facteurs de risque environnementaux impliqués dans la MA sont l’âge, les maladies cardio-vasculaires comme l’hypercholestérolémie, l’hypertension, l’athérosclérose, le diabète, l’obésité, le tabagisme, la dépression, l’inactivité cognitive et physique ou encore un manque d’éducation (pour revues, voir (Leibson et al., 1997 ; Stampfer, 2006 ; Diniz et al., 2013). Parmi ces facteurs, plusieurs études scientifiques démontrent le rôle prépondérant joué par les dérèglements du métabolisme énergétique, et notamment un déficit énergétique cérébral (Yin et al., 2016 ; Butterfield & Halliwell, 2019).
Physiopathologie de la maladie d’Alzheimer
La formation d’agrégats de protéines pathologiques au sein des neurones est un facteur majeur du développement de la MA. De façon précoce, on trouve chez les patients atteints de MA une hyperphosphorylation de la protéine Tau, qui a pour conséquence la formation de dégénérescences neurofibrillaires (Zhang et al., 2021), second signe pathognomique de la MA. Les neurones qui contiennent de la protéine Tau phosphorylée sont alors incapables d’exécuter les fonctions essentielles à la survie d’une cellule nerveuse, et conduisent à une neurodégénérescence. L’accumulation pathologique progressive de protéines Tau phosphorylées est utilisée comme biomarqueur d’évolution de la MA (Wegmann et al., 2021).
On trouve également des dépôts de plaques amyloïdes-β, qui sont fortement toxiques pour le cerveau. Elles favorisent notamment la phosphorylation anormale de la protéine Tau, aggravant la formation d’enchevêtrements neurofibrillaires (Zhang et al., 2021).
Bien que leur présence soit un indicateur post-mortem de la pathologie, le nombre de plaques correspond mal au degré de démence et ne peut donc pas être utilisé comme marqueur pronostic d’évolution de la MA (Majou, 2015).
L’accumulation des plaques amyloïdes et de protéines Tau anormales s’accompagne d’une activation des cellules microgliales, qui sont les macrophages résidents du système nerveux. Ce phénomène va mener à une augmentation des mécanismes neuro-inflammatoires, notamment la sécrétion de cytokines pro-inflammatoires, l’activation de l’inflammasome, du système du complément ou encore des caspases (Akiyama et al., 2000 ; Audinat & Arnoux, 2014 ; Heneka et al., 2015).
Enfin, les substrats énergétiques ainsi que les centrales énergétiques des cellules, les mitochondries, pourraient jouer un rôle important dans la pathogenèse de la MA, en particulier la réduction de l’apport cérébral en glucose et un dysfonctionnement mitochondrial (Perez Ortiz & Swerdlow, 2019).
Implication du déficit énergétique cérébral dans la maladie d’Alzheimer
Rôle des transporteurs au glucose
Alors que le poids du cerveau ne correspond qu’à environ 2 % du poids du corps total, il consomme à lui seul près de 20 % de l’énergie dérivée du glucose, faisant de lui l’organe qui est le plus gros consommateur de glucose (Mergenthaler et al., 2013).
Son transport dans le cerveau est assuré grâce à des glycoprotéines membranaires appelées GLUT (Transporteur de glucose) et plus particulièrement GLUT-1 et -3 qui sont largement exprimées par le cerveau des mammifères (Majou, 2015). Ils jouent un rôle central dans les fonctions cérébrales puisqu’ils assurent un approvisionnement en glucose suffisant en s’adaptant au niveau de glucose disponible et en réponse à l’activité cognitive (Koepsell, 2020). L’évaluation du métabolisme cérébral du glucose par tomographie par émission de positons (PET), montre une réduction de l’absorption du glucose par le cerveau, et plus particulièrement dans les régions les plus vulnérables à la pathologie de la MA (Mosconi, 2005 ; Herholz, 2010). Ainsi, à côté des PET amyloïde et Tau, la mesure de l’absorption du 18F-2-fluoro-2-déoxy-d-glucose, une molécule analogue au glucose, visualisable par PET, est une des mesures spécifiques et sensibles pour l’identification de troubles cognitifs (Mosconi, 2005 ; Blazhenets et al., 2021).
Les atteintes du métabolisme du glucose trouvées chez les patients pourraient être expliquées par une diminution du nombre de récepteurs GLUT-1 et -3 (Simpson et al., 1994 ; An et al., 2018). La déficience en récepteurs GLUT exacerbe les symptômes de la MA car un hypométabolisme général du glucose au niveau du cerveau est responsable d’une réduction de l’activité neuronale (Winkler et al., 2015 ; Nishida et al., 2017 ; Ryu et al., 2019). Cette diminution de l’expression des récepteurs GLUT semble être causée par la toxicité des plaques amyloïdes, bien que les mécanismes sous-jacents restent encore méconnus (Uemura & Greenlee, 2001 ; Zhu et al., 2014).
Rôle de la mitochondrie
Des modifications de la morphologie mitochondriale, une altération de l’activité enzymatique, des atteintes de la chaîne respiratoire et un stress oxydant important sont également observées (Parker, 1991 ; Manczak et al., 2006 ; Du et al., 2010 ; Terada et al., 2020). Ces dommages mitochondriaux sont responsables d’une diminution de la production d’ATP dans le cerveau (Figure 2) (Zhang et al., 2015 ; Ebanks et al., 2020). Les dysfonctions mitochondriales sont des facteurs importants de la neurodégénérescence, et sont retrouvées également dans la maladie de Parkinson (Wu et al., 2019). De façon similaire à la MA, la diminution de la biogénèse mitochondriale, les atteintes à sa fonction, la baisse de la production d’ATP et l’augmentation du stress oxydant, participent à la progression de la maladie de Parkinson (Prasuhn et al., 2021)
Dans la MA, les atteintes mitochondriales sont liées à l’accumulation des dépôts amyloïdes (Manczak et al., 2006 ; Du et al., 2010) et aux protéines Tau anormalement phosphorylées (Cheng & Bai, 2018).
Ainsi, le métabolisme du glucose, de son import jusqu’à son oxydation par les mitochondries, pourrait être une cible potentielle dans la lutte contre le développement de la MA.
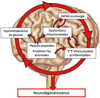 |
Figure 2 Mécanismes impliqués dans la neurodégénescence chez les patients atteints de la maladie d’Alzheimer. Au cœur des mécanismes de neurodégénerescence se trouvent les plaques amyloïdes, responsables de la mise en place d’un cercle vicieux, composé d’un hypométabolisme du glucose, de dysfonctions mitochondriales, d’une augmentation du stress oxydant et des processus inflammatoires, conduisant à un déficit énergétique. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
Prise en charge des patients atteints de la maladie d’Alzheimer
Les premiers médicaments mis sur le marché à la fin du XXème siècle étaient des inhibiteurs d’acétylcholine estérase (Marucci et al., 2021) mais l’insuffisance du service médical rendu font qu’aujourd’hui, ils ne sont plus remboursés par les systèmes de soins.
De nouveaux médicaments sont en cours d’évaluation clinique, notamment pour cibler la neuroinflammation, la protéine Tau ou encore les plaques amyloïdes (Conti Filho et al., 2023). En 2021, l’Aducanumab, un anticorps ciblant les plaques amyloïdes a été approuvé et commercialisé aux Etats-Unis, mais l’Agence Européenne des médicaments a rejeté la demande d’autorisation de ce médicament, faute de preuves cliniques suffisantes (Rahman et al., 2023). Récemment, une étude clinique randomisée a démontré des effets bénéfiques du Donanemab, un anticorps ciblant les fibrilles amyloïdes avant le stade plaque, qui a stoppé la progression de la MA chez 30 à 40 % des patients après 76 semaines de traitement (Sims et al., 2023). Bien que ces résultats soient prometteurs et que la recherche médicamenteuse soit active, un tel traitement curatif pour la MA reste en cours d’évaluation clinique.
La prise en charge médicamenteuse peut être complétée par un suivi psychologique, afin de traiter les troubles psychologiques et comportementaux des patients (Benoit et al., 2003). Il est aussi utile de poursuivre des activités physiques quotidiennes, puisque l’inactivité physique favorise le déclin cognitif, alors que la pratique régulière d’exercices physiques améliore la mémoire (Stephen et al., 2017 ; De la Rosa et al., 2020). Enfin, une prise en charge orthophonique est également proposée, afin de mobiliser les capacités cognitives du patient et de ralentir l’évolution des troubles qui apparaissent dans la MA (Swan et al., 2018).
Cependant, si une prise en charge globale de la MA permet de freiner l’avancée de la pathologie neurodégénérative en maintenant au maximum les capacités du patient, elle n’est à ce jour pas curative (Volkmer et al., 2020) : il pourrait donc être intéressant de la compléter, notamment par une prise en charge nutritionnelle (Figure 3).
Le déficit énergétique, notamment l’hypométabolisme du glucose, est un élément important dans la physiopathologie de la MA, or il n’est pas pris en compte dans les divers versants de la prise en charge du patient. Pourtant, il existe des alimentations protectrices qui agissent sur les facteurs de risque et peuvent ainsi retarder les premiers symptômes et le déclin cognitif (Otaegui-Arrazola et al., 2014 ; Loughman et al., 2021). Parmi ces régimes on trouve l’alimentation cétogène, pauvre en glucides et riche en lipides. Elle présente un indice glycémique faible et permet la production d’autres métabolites utilisables par le cerveau comme les corps cétoniques, qui pourraient induire des effets positifs pour les personnes atteintes de la maladie d’Alzheimer (Rusek et al., 2019).
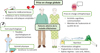 |
Figure 3 Prise en charge globale des patients atteints de la maladie d’Alzheimer. La prise en charge de la maladie d’Alzheimer regroupe différents axes, notamment une approche médicamenteuse, un suivi psychologique, la mise en place d’activités physiques, ou encore un suivi orthophonique. Cette prise en charge pourrait également être renforcée par un encadrement nutritionnel. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
Effets bénéfiques de l’alimentation cétogène enrichie en triglycérides à chaîne moyenne dans la maladie d’Alzheimer
Définition et principes de l’alimentation cétogène
L’alimentation cétogène (KD, Ketogenic Diet), est une alimentation où l’apport en glucides est restreint au maximum (entre 5 et 10 % des apports énergétiques) et où un enrichissement important en lipides assure une couverture suffisante pour les besoins énergétiques du corps (70 à 80 % des apports) (Augustin et al., 2018). Elle s’oppose à l’alimentation moderne où les glucides sont la principale source d’apport énergétique (Figure 4).
Lorsque les glucides sont autant limités, le métabolisme se modifie pour couvrir les besoins énergétiques du cerveau et entre en état de cétose. Le foie produit à partir des acides gras des molécules appelées corps cétoniques, l’acétone est évacuée par voie pulmonaire mais l’acétoacétate et le β-hydroxybutyrate (BHB) rejoignent la circulation sanguine jusqu’au système nerveux. Ils traversent la barrière hémato-encéphalique, pénètrent dans les cellules nerveuses où ils sont retransformés en acétyl-CoA par les mitochondries pour produire de l’ATP (Meyer-Rogge & Meyer-Rogge, 2012) (Figure 5).
Certains acides gras, et plus particulièrement les triglycérides à chaîne moyenne (Medium Chain Triglycerides, MCT), sont plus efficaces pour produire des corps cétoniques. Ils sont présents principalement dans l’huile de coco et les matières grasses laitières. La production de corps cétoniques est significativement supérieure lors de la consommation de MCT par rapport aux triglycérides à chaîne longue classiquement trouvés par exemple dans l’huile d’olive ou de colza (Harvey et al., 2018 ; Norgren et al., 2020). Grâce à leur courte chaîne carbonée, ils traversent directement la membrane des entérocytes lors de la digestion et sont importés dans le foie où ils sont plus rapidement métabolisés en acétyl-CoA puis transformés en corps cétoniques (Schönfeld & Wojtczak, 2016). Ainsi, une alimentation KD enrichie en MCT pourrait être plus efficace pour induire un état de cétose (Bach et al., 1977 ; Liu & Wang, 2013).
À l’origine, l’alimentation KD a été mise au point en 1921 par le docteur Russell Wilder afin de traiter les épilepsies pédiatriques résistantes aux médicaments. La consommation d’une alimentation KD apparaît plus efficace pour réduire les crises d’épilepsie que l’utilisation d’anticonvulsifs (Wirrell et al., 2018 ; Lyons et al., 2020). Les effets bénéfiques du KD dans l’épilepsie semblerait passer par un effet neuroprotecteur des corps cétoniques (Gough et al., 2021 ; Wang et al., 2023). Ces dernières années, l’alimentation KD est plus fréquemment proposée dans la prise en charge de pathologies métaboliques, telles l’obésité, le diabète de type 2 ou encore certains cancers (Charlot et al., 2021 ; Kumar et al., 2021). Ainsi, l’alimentation KD pourrait présenter un intérêt dans la prise en charge de la MA (Hersant & Grossberg, 2022 ; Wang et al., 2023).
 |
Figure 4 Répartition des macronutriments de l’alimentation moderne versus l’alimentation cétogène. L’alimentation moderne est une alimentation où les glucides et les lipides occupent une part importante des macronutriments, alors que l’alimentation cétogène présente une restriction importante de la part des glucides et un enrichissement en lipides. |
 |
Figure 5 Utilisation des corps cétoniques comme substrat énergétique pour le cerveau. Les corps cétoniques sont produits par les mitochondries du foie à partir de l’Acétyl-CoA puis sécrétés dans la circulation sanguine. Ils sont ainsi transportés jusqu’au cerveau où ils sont transformés à nouveau en Acétyl-CoA, qui pourra entrer dans le cycle de Krebs pour produire de l’ATP. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
Mécanismes neuroprotecteurs de l’alimentation cétogène
L’augmentation de la production de corps cétoniques par le foie est l’élément clé dans les effets neuroprotecteurs de l’alimentation KD. L’apport important en corps cétoniques, encore augmenté lorsque l’alimentation KD est enrichie en MCT, pallie le déficit énergétique provoqué par l’hypométabolisme général du glucose au niveau neuronal et assure un apport en ATP suffisant au cerveau (Jensen et al., 2020 ; Lilamand et al., 2022 ; Castro et al., 2023). Plusieurs études ont montré que l’augmentation de la production de corps cétoniques par une supplémentation en MCT améliorait le métabolisme énergétique du cerveau ainsi que les scores de certains tests cognitifs, témoignant d’une amélioration des capacités cognitives chez des patients atteints de la MA (Reger et al., 2004 ; Croteau et al., 2018 ; Fortier et al., 2019 ; Ota et al., 2019). Une autre étude, réalisée sur 10 patients atteints de MA, démontre que 3 mois d’alimentation KD enrichie en MCT étaient associés à une production significative de corps cétoniques et à une amélioration de leurs scores cognitifs mais à la perte des effets bénéfiques après l’arrêt du régime et le retour à une alimentation habituelle (Taylor et al., 2018).
Enfin, l’étude de Krikorian et al. (2012) s’est intéressée à la comparaison des effets entre une alimentation riche en glucides versus une alimentation KD sur les capacités cognitives de personnes âgées avec une déficience cognitive légère. Dans ce groupe de sujets, seule l’alimentation KD avait un effet positif sur la mémoire, et ces résultats étaient corrélés positivement avec les niveaux de corps cétoniques. Une amélioration de la fonction neurocognitive par l’alimentation KD pourrait donc retarder la neurodégénérescence précoce.
Les corps cétoniques, en plus de permettre une couverture énergétique cérébrale suffisante, présentent de nombreux effets neuroprotecteurs en modulant l’activité des cellules immunitaires (Benito et al., 2020). Le BHB peut se fixer à des récepteurs présents à la surface des macrophages et des cellules microgliales et les activer. Ces récepteurs régulent ainsi la fonction de ces cellules et agissent notamment sur une population de macrophages au phénotype neuroprotecteur (Zandi-Nejad et al., 2013 ; Rahman et al., 2014). Parmi les autres mécanismes neuroprotecteurs des corps cétoniques, on retrouve leur propriété antioxydante. Plusieurs études réalisées sur des modèles in vitro et in vivo ont montré que le BHB pouvait capter les dérivés réactifs de l’oxygène, diminuant ainsi le stress oxydant (Haces et al., 2008 ; Xie et al., 2015 ; Rojas-Morales et al., 2020). Chez le rat, les corps cétoniques ont permis une diminution des plaques amyloïdes et du stress oxydant, notamment en augmentant l’activité des enzymes antioxydantes (Ziegler et al., 2003 ; Xie et al., 2015).
L’alimentation cétogène module également l’inflammation, puisque les lipides, déclenchent l’activation de la voie de signalisation du facteur nucléaire kappa-B (NF-κB). Cette voie contrôle un grand nombre de gènes impliqués dans l’inflammation, ce qui permet de la réduire via une diminution de la sécrétion des cytokines pro-inflammatoires (Straus & Glass, 2007 ; Hou et al., 2012 ; Dupuis et al., 2015). Un autre mécanisme anti-inflammatoire est médié par le BHB. Ce corps cétonique inhibe l’inflammasome, un complexe protéique impliqué dans les processus inflammatoires, induisant de cette façon une diminution de la sécrétion de cytokines pro-inflammatoires (Youm et al., 2015 ; Goldberg et al., 2017 ; Shippy et al., 2020 ; Kong et al., 2022). Par ailleurs, chez les souris, la prise d’une alimentation cétogène réduit les niveaux de cytokines pro-inflammatoires dans le système nerveux (Yang & Cheng, 2010 ; Xu et al., 2022).
Enfin, l’alimentation cétogène ainsi que les MCT, pourraient agir positivement sur le métabolisme mitochondrial. La consommation de MCT augmente l’expression des protéines mitochondriales, notamment celles de la chaîne respiratoire, ainsi que les acteurs de la biogénèse mitochondriale (Turner et al., 2009 ; Wang et al., 2018 ; Hasan-Olive et al., 2019 ; Charlot et al., 2022 ; Gómora-García et al., 2023).
Ainsi, l’alimentation cétogène, d’autant plus si elle est enrichie en MCT, semble être une stratégie prometteuse dans la lutte contre la MA. En assurant au cerveau un apport suffisant en énergie, réduisant le stress oxydant et augmentant les capacités mitochondriales, elle pourrait agir sur plusieurs facteurs clés de la pathogenèse de la maladie, à savoir l’hypométabolisme du glucose, le déficit énergétique, l’inflammation et les dysfonctions mitochondriales (Figure 6). Ainsi, une prise nutritionnelle combinée aux traitements actuels pourrait améliorer les scores de tests cognitifs, et induire une meilleure compensation des troubles neurodégénératifs chez les patients atteints de la MA (Reger et al., 2004 ; Krikorian et al., 2012 ; Croteau et al., 2018 ; Taylor et al., 2018 ; Fortier et al., 2019 ; Ota et al., 2019).
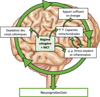 |
Figure 6 Mécanismes de neuroprotection médiés par l’alimentation cétogène enrichie en MCT. L’alimentation cétogène enrichie en MCT permet de lutter contre l’hypométabolisme du glucose grâce à la production de corps cétoniques, qui assurent un apport suffisant en substrats énergétiques au cerveau. Elle permet aussi d’améliorer les capacités mitochondriales, de réduire le stress oxydant et l’inflammation, ce qui est également bénéfique pour protéger les capacités oxydatives mitochondriales. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
Limites et perspectives
Même si l’alimentation cétogène paraît être une approche complémentaire intéressante pour lutter contre l’avancée de la MA, les études qui évaluent ses effets dans la MA restent encore peu nombreuses, sur des effectifs restreints, sans contrôle à long terme (Hersant & Grossberg, 2022). De plus, ce type d’alimentation restrictive présente des limites. Les effets secondaires mineurs les plus courants sont nausées, vomissements, maux de tête, fatigue, ou encore étourdissements. Ces symptômes étant causés par l’adaptation du métabolisme à la production de corps cétoniques, ils diminuent et disparaissent en quelques jours (Yuan et al., 2020 ; Moriconi et al., 2021). D’autres effets secondaires ont été rapportés au niveau de la santé cardio-métabolique avec une augmentation des marqueurs du métabolisme lipidique, une résistance à l’insuline ou encore une légère atrophie musculaire (Bielohuby et al., 2013 ; Ellenbroek et al., 2014 ; Grandl et al., 2018 ; Nakao et al., 2019). Cependant, ces effets négatifs sont principalement retrou-vés dans des études sur des modèles animaux ou lorsque le régime appliqué n’est pas correctement équilibré. Les études chez l’Homme montrent globalement une bonne tolérance de cette alimentation sans effets secondaires graves (Sumithran & Proietto, 2008 ; Włodarek, 2019 ; Alarim et al., 2020 ; Goss et al., 2020 ; Yuan et al., 2020 ; Charlot & Zoll, 2022).
La limite la plus importante du régime cétogène est la faible observance sur le long terme et la difficulté de maintenir un régime sans sucres ni glucides. En effet, les personnes âgées voient leur métabolisme se modifier, ce qui a un impact sur leur prise alimentaire (Drewnowski & Shultz, 2001). Physiologiquement, le goût et l’odorat diminuent, c’est pourquoi les personnes âgées se dirigent davantage vers des aliments au goût prononcé (Kondo et al., 2020). Ces personnes, et particulièrement les patients atteints de la MA, choisissent les aliments qui leur procurent du plaisir, et montrent une préférence pour les produits sucrés (Greenwood & Parrott, 2017 ; Whitelock & Ensaff, 2018). De même, la dénutrition des personnes âgées est un point important à surveiller et les recommandations de la Haute Autorité de Santé préconisent de ne pas réduire le sucre et les glucides de manière drastique, ce qui pourrait avoir un effet anorexigène (Haute Autorité de Santé, 2007). Comme l’alimentation cétogène proscrit le sucre, il s’agit donc d’une limite importante, nécessitant un encadrement strict des médecins et diététiciens pour limiter tout risque pour le patient et permettant d’expliquer aux malades et aux aidants les effets positifs de l’alimentation, d’indiquer les aliments autorisés et interdits et de suivre l’évolution de la santé du patient au quotidien.
Au vu de ces limites, il serait peut-être plus intéressant de proposer entre les cures de régime cétogène, un régime alimentaire plus souple qui pourrait être préconisé une ou deux fois par an durant un temps limité (maximum de quelques semaines/mois). Néanmoins, tout cela reste empirique et demande à être validé par des études menées chez des patients à différents stades de la maladie. Par exemple, le régime Atkins utilise le même processus de cétose tout en étant moins restrictif au niveau de la répartition des macronutriments. Une étude montre que la prise d’une alimentation Atkins chez des patients atteints de la MA à un stade peu avancé permet d’améliorer la mémoire épisodique et la vitalité (Brandt et al., 2019). Enfin, il pourrait être pertinent, sur du long terme, d’enrichir l’alimentation des patients en MCT. En effet, les MCT seuls sont capables d’augmenter la production de corps cétoniques et d’améliorer les capacités cognitives (Reger et al., 2004 ; Croteau et al., 2018 ; Fortier et al., 2019 ; Ota et al., 2019). Ainsi, la prise d’une gélule de MCT quotidienne pourrait être plus facile à mettre en place pour augmenter la production de corps cétoniques qu’une alimentation cétogène stricte.
Conclusions générales
Aujourd’hui, les études évaluant l’efficacité de l’alimentation cétogène dans la MA restent trop peu nombreuses, et les protocoles manquent de standardisation. Il n’existe pas pour le moment de consensus quant à la durée ou le type de régime (cétogène enrichi ou non en MCT, régime Atkins…) à utiliser pour que les effets bénéfiques sur la MA soient optimaux. De plus, ces approches doivent être testées aux différents stades de la MA afin de savoir à quel moment proposer une prise en charge nutritionnelle au patient. Le terrain de recherche dans ce domaine est vaste, les contraintes sont nombreuses et il reste encore à répondre à de nombreuses questions avant de pouvoir réellement établir les bénéfices de cette alimentation pour l’évolution de la MA et pour proposer cette approche en routine aux patients (Włodarek, 2019).
Déclaration de liens d’intérêts
L’équipe de Joffrey Zoll est financée en partie par l’industriel STEPAN et l’Université de Strasbourg.
Remerciements
Nous remercions Christèle Carli-Basset, Orthophoniste à Montlouis-sur-Loire, pour son aide dans la relecture et correction linguistique de cette revue.
Références
- Akiyama, H., Barger, S., Barnum, S., Bradt, B., Bauer, J., Cole, G. M., Cooper, N. R., Eikelenboom, P., Emmerling, M., Fiebich, B. L., Finch, C. E., Frautschy, S., Griffin, W. S. T., Hampel, H., Hull, M., Landreth, G., Lue, L., Mrak, R., Mackenzie, I. R., McGeer, P.L., O’Banion, M. K., Pachter, J., Pasinetti, G., Plata-Salaman, C., Rogers, J., Rydel, R., Shen, Y., Streit, W., Strohmeyer, R., Tooyoma, I., Van Muiswinkel, F. L., Veerhuis, R., Walker, D., Webster, S., Wegrzyniak, B., Wenk, G., Wyss-Coray, T. (2000). Inflammation and Alzheimer’s disease. Neurobiol Aging, 21, 383-421. [CrossRef] [PubMed] [Google Scholar]
- Alarim, R.A., Alasmre, F.A., Alotaibi, H.A., Alshehri, M.A., Hussain, S.A. (2020). Effects of the Ketogenic Diet on Glycemic Control in Diabetic Patients: Meta-Analysis of Clinical Trials. Cureus, 12, e10796. [PubMed] [Google Scholar]
- An, Y., Varma, V. R., Varma, S., Casanova, R., Dammer, E., Pletnikova, O., Chia, C. W., Egan, J. M., Ferrucci, L., Troncoso, J., Levey, A. I., Lah, J., Seyfried, N. T., Legido-Quigley, C., O’Brien, R., Thambisetty, M. (2018). Evidence for brain glucose dysregulation in Alzheimer’s disease. Alzheimers Dement, 14, 318-329. [CrossRef] [PubMed] [Google Scholar]
- Audinat, É., Arnoux, I. (2014). La microglie : des cellules immunitaires qui sculptent et contrôlent les synapses neuronales. Med Sci, 30, 153-159. [Google Scholar]
- Augustin, K., Khabbush, A., Williams, S., Eaton, S., Orford, M., Cross, J. H., Heales, S.J.R., Walker, M.C., Williams, R.S.B. (2018). Mechanisms of action for the medium-chain triglyceride ketogenic diet in neurological and metabolic disorders. Lancet Neurol, 17, 84-93. [CrossRef] [PubMed] [Google Scholar]
- Bach, A., Schirardin, H., Weryha, A., Bauer, M. (1977). Ketogenic Response to Medium-Chain Triglyceride Load in the Rat. J Nutr, 107, 1863-1870. [CrossRef] [PubMed] [Google Scholar]
- Benito, A., Hajji, N., O’Neill, K., Keun, H. C., Syed, N. (2020). β-Hydroxybutyrate Oxidation Promotes the Accumulation of Immunometabolites in Activated Microglia Cells. Metabolites, 26, 346. [CrossRef] [PubMed] [Google Scholar]
- Benoit, M., Staccini, P., Brocker, P., Benhamidat, T., Bertogliati, C., Lechowski, L., Tortrat, D., Robert, P. H. (2003). Symptômes comportementaux et psychologiques dans la maladie d’ Alzheimer : Résultats de l’étude REAL.FR. Rev Med Interne, 24, 319s-324s. [CrossRef] [PubMed] [Google Scholar]
- Bielohuby, M., Sisley, S., Sandoval, D., Herbach, N., Zengin, A., Fischereder, M., Menhofer, D., Stoehr, B.J.M., Stemmer, K., Wanke, R., Tschöp, M.H., Seeley, R.J., Bidlingmaier, M. (2013). Impaired glucose tolerance in rats fed low-carbohydrate, high-fat diets. Am J Physiol Endocrinol Metab., 305, E1059-E1070. [CrossRef] [PubMed] [Google Scholar]
- Blazhenets, G., Frings, L., Ma, Y., Sörensen, A., Eidelberg, D., Wiltfang, J., Meyer, P.T., for the Alzheimer’s Disease Neuroimaging Initiative. (2021). Validation of the Alzheimer Disease Dementia Conversion-Related Pattern as an ATN Biomarker of Neurodegeneration. Neurology, 96, e1358-e1368. [CrossRef] [PubMed] [Google Scholar]
- Brandt, J., Buchholz, A., Henry-Barron, B., Vizthum, D., Avramopoulos, D., Cervenka, M. C. (2019). Preliminary Report on the Feasibility and Efficacy of the Modified Atkins Diet for Treatment of Mild Cognitive Impairment and Early Alzheimer’s Disease. J Alzheimers Dis, 68, 969-981. [CrossRef] [PubMed] [Google Scholar]
- Butterfield, D. A., Halliwell, B. (2019). Oxidative stress, dysfunctional glucose metabolism and Alzheimer disease. Nat Rev Neurosci, 20, 148-160. [CrossRef] [PubMed] [Google Scholar]
- Castro, C.B., Dias, C.B., Hillebrandt, H., Sohrabi, H.R., Chatterjee, P., Shah, T.M., Fuller, S.J., Garg, M.L., Martins, R.N. (2023). Medium-chain fatty acids for the prevention or treatment of Alzheimer’s disease : a systematic review and meta-analysis. Nutr Rev, nuac104. [Google Scholar]
- Charlot, A., Conrad, O., Zoll, J. (2020). Le régime cétogène : une stratégie alimentaire efficace en complément des traitements contre le cancer ? Biol Aujourdhui, 214, 115-123. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Charlot, A., Boumiza, R., Roux, M., Zoll, J. (2021). Obésité, inflammation et COVID-19 : intérêt préventif de l’alimentation cétogène ? Biol Aujourdhui, 215, 63-72. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Charlot, A., Morel, L., Bringolf, A., Georg, I., Charles, A.L., Goupilleau, F., Geny, B., Zoll, J. (2022). Octanoic Acid-Enrichment Diet Improves Endurance Capacity and Reprograms Mitochondrial Biogenesis in Skeletal Muscle of Mice. Nutrients, 14, 2721. [CrossRef] [PubMed] [Google Scholar]
- Charlot, A., Zoll, J. (2022). Beneficial Effects of the Ketogenic Diet in Metabolic Syndrome: A Systematic Review. Diabetology, 3, 292-309. [CrossRef] [Google Scholar]
- Cheng, Y., Bai, F. (2018). The Association of Tau with Mitochondrial Dysfunction in Alzheimer’s Disease. Front Neurosci, 12, 163. [CrossRef] [PubMed] [Google Scholar]
- Conti Filho, C.E., Loss, L.B., Marcolongo-Pereira, C., Rossoni Junior, J.V., Barcelos, R.M., Chiarelli-Neto, O., da Silva, B.S., Passamani Ambrosio, R., Castro, F.C.A.Q., Teixeira, S.F., Mezzomo, N.J. (2023). Advances in Alzheimer’s disease’s pharmacological treatment. Front Pharmacol, 26, 14, 1101452. [CrossRef] [PubMed] [Google Scholar]
- Croteau, E., Castellano, C.-A., Richard, M. A., Fortier, M., Nugent, S., Lepage, M., Duchesne, S., Whittingstall, K., Turcotte, É. E., Bocti, C., Fülöp, T., Cunnane, S. C. (2018). Ketogenic Medium Chain Triglycerides Increase Brain Energy Metabolism in Alzheimer’s Disease. J Alzheimers Dis, 64, 551-561. [CrossRef] [PubMed] [Google Scholar]
- De la Rosa, A., Olaso-Gonzalez, G., Arc-Chagnaud, C., Millan, F., Salvador-Pascual, A., García-Lucerga, C., Blasco-Lafarga, C., Garcia-Dominguez, E., Carretero, A., Correas, A.G., Viña, J., Gomez-Cabrera, M. C. (2020). Physical exercise in the prevention and treatment of Alzheimer’s disease. J Sport Health Sci, 9, 394-404. [CrossRef] [PubMed] [Google Scholar]
- Diniz, B.S., Butters, M.A., Albert, S.M., Dew, M.A., Reynolds, C.F. (2013). Late-life depression and risk of vascular dementia and Alzheimer’s disease: Systematic review and meta-analysis of community-based cohort studies. Br J Psychiatry, 202, 329-335. [CrossRef] [PubMed] [Google Scholar]
- Drewnowski, A., Shultz, J. M. (2001). Impact of aging on eating behaviors, food choices, nutrition, and health status. J Nutr Health Aging, 5, 75-79. [PubMed] [Google Scholar]
- Du, H., Guo, L., Yan, S., Sosunov, A.A., McKhann, G.M., Shi Du Yan, S. (2010). Early deficits in synaptic mitochondria in an Alzheimer’s disease mouse model. Proc Natl Acad Sci USA, 107, 18670-18675. [CrossRef] [PubMed] [Google Scholar]
- Dupuis, N., Curatolo, N., Benoist, J.-F., Auvin, S. (2015). Ketogenic diet exhibits anti-inflammatory properties. Epilepsia, 56, e95-e98. [PubMed] [Google Scholar]
- Ebanks, B., Ingram, T.L., Chakrabarti, L. (2020). ATP synthase and Alzheimer’s disease: Putting a spin on the mitochondrial hypothesis. Aging (Albany NY), 12, 16647-16662. [CrossRef] [PubMed] [Google Scholar]
- Ellenbroek, J.H., van Dijck, L., Töns, H.A., Rabelink, T.J., Carlotti, F., Ballieux, B.E.P.B., de Koning, E.J.P. (2014). Long-term ketogenic diet causes glucose intolerance and reduced β- and α-cell mass but no weight loss in mice. Am J Physiol Endocrinol Metab, 306, E552-E558. [CrossRef] [PubMed] [Google Scholar]
- Fortier, M., Castellano, C.-A., Croteau, E., Langlois, F., Bocti, C., St-Pierre, V., Vandenberghe, C., Bernier, M., Roy, M., Descoteaux, M., Whittingstall, K., Lepage, M., Turcotte, É.E., Fulop, T., Cunnane, S.C. (2019). A ketogenic drink improves brain energy and some measures of cognition in mild cognitive impairment. Alzheimers Dement, 15, 625-634. [CrossRef] [PubMed] [Google Scholar]
- Gatz, M., Reynolds, C.A., Fratiglioni, L., Johansson, B., Mortimer, J.A., Berg, S., Fiske, A., Pedersen, N.L. (2006). Role of Genes and Environments for Explaining Alzheimer Disease. Arch Gen Psychiatry, 63, 168. [CrossRef] [PubMed] [Google Scholar]
- Goldberg, E.L., Asher, J.L., Molony, R.D., Shaw, A.C., Zeiss, C.J., Wang, C., Morozova-Roche, L.A., Herzog, R.I., Iwasaki, A., Dixit, V. D. (2017). β-Hydroxybutyrate Deactivates Neutrophil NLRP3 Inflammasome to Relieve Gout Flares. Cell Rep, 18, 2077-2087. [CrossRef] [PubMed] [Google Scholar]
- Gómora-García, J.C., Montiel, T., Hüttenrauch, M., Salcido-Gómez, A., García-Velázquez, L., Ramiro-Cortés, Y., Gomora, J.C., Castro-Obregón, S., Massieu, L. (2023). Effect of the Ketone Body, D-β-Hydroxybutyrate, on Sirtuin2-Mediated Regulation of Mitochondrial Quality Control and the Autophagy-Lysosomal Pathway. Cells, 12, 486. [CrossRef] [PubMed] [Google Scholar]
- Goss, A.M., Gower, B., Soleymani, T., Stewart, M., Pendergrass, M., Lockhart, M., Krantz, O., Dowla, S., Bush, N., Garr Barry, V., Fontaine, K.R. (2020). Effects of weight loss during a very low carbohydrate diet on specific adipose tissue depots and insulin sensitivity in older adults with obesity: A randomized clinical trial. Nutr Metab (Lond), 17, 64. [CrossRef] [PubMed] [Google Scholar]
- Gough, S.M., Casella, A., Ortega, K.J., Hackam, A.S. (2021). Neuroprotection by the Ketogenic Diet : Evidence and Controversies. Front Nutr, 8, 782657. [CrossRef] [PubMed] [Google Scholar]
- Grandl, G., Straub, L., Rudigier, C., Arnold, M., Wueest, S., Konrad, D., Wolfrum, C. (2018). Short-term feeding of a ketogenic diet induces more severe hepatic insulin resistance than an obesogenic high-fat diet. J Physiol, 596, 4597-4609. [CrossRef] [PubMed] [Google Scholar]
- Greenwood, C.E., Parrott, M.D. (2017). Nutrition as a component of dementia risk reduction strategies. Health Manage Forum, 30, 40-45. [CrossRef] [PubMed] [Google Scholar]
- Haces, M.L., Hernández-Fonseca, K., Medina-Campos, O.N., Montiel, T., Pedraza-Chaverri, J., Massieu, L. (2008). Antioxidant capacity contributes to protection of ketone bodies against oxidative damage induced during hypoglycemic conditions. Exp Neurol, 211, 85-96. [CrossRef] [PubMed] [Google Scholar]
- Harvey, C.C.J., Schofield, G.M., Williden, M., McQuillan, J.A. (2018). The Effect of Medium Chain Triglycerides on Time to Nutritional Ketosis and Symptoms of Keto-Induction in Healthy Adults: A Randomised Controlled Clinical Trial. J Nutr Metab, 2018, 2630565. [CrossRef] [Google Scholar]
- Hasan-Olive, M.M., Lauritzen, K.H., Ali, M., Rasmussen, L.J., Storm-Mathisen, J.,Bergersen, L.H. (2019). A Ketogenic Diet Improves Mitochondrial Biogenesis and Bioenergetics via the PGC1α-SIRT3-UCP2 Axis. Neurochem Res, 44, 22-37. [CrossRef] [PubMed] [Google Scholar]
- Haute Autorité de Santé [Internet]. (2007). Stratégie de prise en charge en cas de dénutrition protéino-énergétique chez la personne âgée. Haute Autorité de Santé. Disponible sur : https://www.has-sante.fr/jcms/c_546549/fr/strategie-de-prise-en-charge-en-cas-de-denutrition-proteino-energetique-chez-la-personne-agee. [Google Scholar]
- Heneka, M.T., Carson, M.J., El Khoury, J., Landreth, G.E., Brosseron, F., Feinstein, D.L., Jacobs, A.H., Wyss-Coray, T., Vitorica, J., Ransohoff, R.M., Herrup, K., Frautschy, S.A., Finsen, B., Brown, G.C., Verkhratsky, A., Yamanaka, K., Koistinaho, J., Latz, E., Halle, A., Petzold, G.C., Town, T., Morgan, D., Shinohara, M.L., Perry, V.H., Holmes, C., Bazan, N.G., Brooks, D.J., Hunot, S., Joseph, B., Deigendesch, N., Garaschuk, O., Boddeke, E., Dinarello, C.A., Breitner, J.C., Cole, G.M., Golenbock, D.T., Kummer, M.P. (2015). Neuroinflammation in Alzheimer’s Disease. Lancet Neurol, 14, 388-405. [CrossRef] [PubMed] [Google Scholar]
- Herholz, K. (2010). Cerebral glucose metabolism in preclinical and prodromal Alzheimer’s disease. Expert Rev Neurother, 10, 1667-1673. [CrossRef] [PubMed] [Google Scholar]
- Hersant, H., Grossberg, G. (2022). The Ketogenic Diet and Alzheimer’s Disease. J Nutr Health Aging, 26, 606–614. [CrossRef] [PubMed] [Google Scholar]
- Hou, Y., Moreau, F., Chadee, K. (2012). PPARγ is an E3 ligase that induces the degradation of NFκB/p65. Nat Commun, 3, 1300. [CrossRef] [PubMed] [Google Scholar]
- INSERM [Internet]. (2006). Orphanet : syndrome de déficit en transporteur du glucose de type 1, forme classique. Disponible sur : https://www.orpha.net/consor/cgi-bin/OC_Exp.php?Lng=FR&Expert=71277. [Google Scholar]
- Jack, C.R., Bennett, D.A., Blennow, K., Carrillo, M.C., Dunn, B., Haeberlein, S.B., Holtzman, D.M., Jagust, W., Jessen, F., Karlawish, J., Liu, E., Molinuevo, J.L., Montine, T., Phelps, C., Rankin, K. P., Rowe, C.C., Scheltens, P., Siemers, E., Snyder, H.M., Sperling, R. (2018). NIA-AA Research Framework: Toward a biological definition of Alzheimer’s disease. Alzheimers Dement, 14, 535-562. [CrossRef] [PubMed] [Google Scholar]
- Jensen, N. J., Wodschow, H. Z., Nilsson, M., Rungby, J. (2020). Effects of Ketone Bodies on Brain Metabolism and Function in Neurodegenerative Diseases. Int J Mol Sci, 21, 8767. [CrossRef] [PubMed] [Google Scholar]
- Koepsell, H. (2020). Glucose transporters in brain in health and disease. Pflügers Arch, 472, 1299-1343. [CrossRef] [PubMed] [Google Scholar]
- Kondo, K., Kikuta, S., Ueha, R., Suzukawa, K., Yamasoba, T. (2020). Age-Related Olfactory Dysfunction: Epidemiology, Pathophysiology, and Clinical Management. Front Aging Neurosci, 12, 208. [CrossRef] [PubMed] [Google Scholar]
- Kong, G., Wang, J., Li, R., Huang, Z., Wang, L. (2022). Ketogenic diet ameliorates inflammation by inhibiting the NLRP3 inflammasome in osteoarthritis. Arthritis Res Ther, 24, 113. [CrossRef] [PubMed] [Google Scholar]
- Krikorian, R., Shidler, M.D., Dangelo, K., Couch, S.C., Benoit, S.C., Clegg, D.J. (2012). Dietary ketosis enhances memory in mild cognitive impairment. Neurobiol Aging, 33, 425.e19-425.e27. [CrossRef] [PubMed] [Google Scholar]
- Kumar, S., Behl, T., Sachdeva, M., Sehgal, A., Kumari, S., Kumar, A., Kaur, G., Yadav, H.N., Bungau, S. (2021). Implicating the effect of ketogenic diet as a preventive measure to obesity and diabetes mellitus. Life Sci, 264, 118661. [CrossRef] [PubMed] [Google Scholar]
- Leibson, C.L., Rocca, W.A., Hanson, V.A., Cha, R., Kokmen, E., O’Brien, P. C., Palumbo, P.J. (1997). Risk of dementia among persons with diabetes mellitus: A population-based cohort study. Am J Epidemiol, 145, 301-308. [CrossRef] [PubMed] [Google Scholar]
- Lilamand, M., Mouton-Liger, F., Di Valentin, E., Sànchez Ortiz, M., Paquet, C. (2022). Efficacy and Safety of Ketone Supplementation or Ketogenic Diets for Alzheimer’s Disease: A Mini Review. Front Nutr, 8, 807970. [CrossRef] [PubMed] [Google Scholar]
- Liu, Y. C., Wang, H.-S. (2013). Medium-chain triglyceride ketogenic diet, an effective treatment for drug-resistant epilepsy and a comparison with other ketogenic diets. Biomed J, 36, 9-15. [CrossRef] [PubMed] [Google Scholar]
- Loughman, A., Staudacher, H. M., Rocks, T., Ruusunen, A., Marx, W., O Apos Neil, A., Jacka, F.N. (2021). Diet and Mental Health. Mod Trends Psychiatry, 32, 100-112. [CrossRef] [PubMed] [Google Scholar]
- Lyons, L., Schoeler, N.E., Langan, D., Cross, J. H. (2020). Use of ketogenic diet therapy in infants with epilepsy : A systematic review and meta-analysis. Epilepsia, 61, 1261-1281 [CrossRef] [PubMed] [Google Scholar]
- Majou, D. (2015). Alzheimer’s disease: Origins, mechanisms, people at risk and prevention by DHA (omega-3 fatty acid). Actia Editions. [Google Scholar]
- Manczak, M., Anekonda, T.S., Henson, E., Park, B.S., Quinn, J., Reddy, P.H. (2006). Mitochondria are a direct site of a beta accumulation in Alzheimer’s disease neurons: Implications for free radical generation and oxidative damage in disease progression. Hum Mol Genet, 15, 1437-1449. [CrossRef] [PubMed] [Google Scholar]
- Marucci, G., Buccioni, M., Ben, D.D., Lambertucci, C., Volpini, R., Amenta, F. (2021). Efficacy of acetylcholinesterase inhibitors in Alzheimer’s disease. Neuropharmacology, 190, 108352. [CrossRef] [PubMed] [Google Scholar]
- Mergenthaler, P., Lindauer, U., Dienel, G. A., Meisel, A. (2013). Sugar for the brain: The role of glucose in physiological and pathological brain function. Trends Neurosci, 36, 587-597. [CrossRef] [PubMed] [Google Scholar]
- Meyer-Rogge, S., Meyer-Rogge, K. (2012). Biochimie métabolique. De Boeck. ISBN 978-2-8041-7147-6 [Google Scholar]
- Moriconi, E., Camajani, E., Fabbri, A., Lenzi, A., Caprio, M. (2021). Very-Low-Calorie Ketogenic Diet as a Safe and Valuable Tool for Long-Term Glycemic Management in Patients with Obesity and Type 2 Diabetes. Nutrients, 13, 758. [CrossRef] [PubMed] [Google Scholar]
- Mosconi, L. (2005). Brain glucose metabolism in the early and specific diagnosis of Alzheimers disease: FDG-PET studies in MCI and AD. Eur J Nucl Med Mol Imaging, 32, 486-510. [CrossRef] [MathSciNet] [PubMed] [Google Scholar]
- Nakao, R., Abe, T., Yamamoto, S., Oishi, K. (2019). Ketogenic diet induces skeletal muscle atrophy via reducing muscle protein synthesis and possibly activating proteolysis in mice. Sci Rep, 9, 19652. [CrossRef] [PubMed] [Google Scholar]
- Nishida, Y., Winkler, E., Sagare, A., De Vivo, D., Zlokovic, B. (2017). Decreased glucose transporter 1 expression at the blood-brain barrier exacerbates Alzheimer disease-like phenotypes in mouse models. J Neurol Sci, 381, 768. [CrossRef] [Google Scholar]
- Norgren, J., Sindi, S., Sandebring-Matton, A., Kåreholt, I., Daniilidou, M., Akenine, U., Nordin, K., Rosenborg, S., Ngandu, T., Kivipelto, M. (2020). Ketosis after Intake of Coconut Oil and Caprylic Acid—With and Without Glucose: A Cross-Over Study in Healthy Older Adults. Front Nutr, 7, 40. [CrossRef] [PubMed] [Google Scholar]
- Organisation mondiale de la santé [Internet]. (2020). La démence. Organisation mondiale de la santé. Disponible sur : https://www.who.int/fr/news-room/fact-sheets/detail/dementia. [Google Scholar]
- Ota, M., Matsuo, J., Ishida, I., Takano, H., Yokoi, Y., Hori, H., Yoshida, S., Ashida, K., Nakamura, K., Takahashi, T., Kunugi, H. (2019). Effects of a medium-chain triglyceride-based ketogenic formula on cognitive function in patients with mild-to-moderate Alzheimer’s disease. Neurosci Lett, 690, 232-236. [CrossRef] [PubMed] [Google Scholar]
- Otaegui-Arrazola, A., Amiano, P., Elbusto, A., Urdaneta, E., Martínez-Lage, P. (2014). Diet, cognition, and Alzheimer’s disease: Food for thought. Eur J Nutr, 53, 1-23. [CrossRef] [Google Scholar]
- Parker, W. D. (1991). Cytochrome oxidase deficiency in Alzheimer’s disease. Ann N Y Acad Sci, 640, 59-64. [CrossRef] [PubMed] [Google Scholar]
- Perez Ortiz, J.M., Swerdlow, R.H. (2019). Mitochondrial dysfunction in Alzheimer’s disease: Role in pathogenesis and novel therapeutic opportunities. Br J Pharmacol, 176, 3489-3507. [CrossRef] [PubMed] [Google Scholar]
- Prasuhn, J., Davis, R.L., Kumar, K.R. (2021). Targeting Mitochondrial Impairment in Parkinson’s Disease : Challenges and Opportunities. Front Cell Dev Biol, 8, 615461. [CrossRef] [PubMed] [Google Scholar]
- Rahman, M., Muhammad, S., Khan, M.A., Chen, H., Ridder, D.A., Müller-Fielitz, H., Pokorná, B., Vollbrandt, T., Stölting, I., Nadrowitz, R., Okun, J. G., Offermanns, S., Schwaninger, M. (2014). The β-hydroxybutyrate receptor HCA 2 activates a neuroprotective subset of macrophages. Nat Commun, 5, 1-11. [CrossRef] [Google Scholar]
- Rahman, A., Hossen, M.A., Chowdhury, M.F.I., Bari, S., Tamanna, N., Sultana, S.S., Haque, S.N., Al Masud, A., Saif-Ur-Rahman, K.M. (2023). Aducanumab for the treatment of Alzheimer’s disease : a systematic review. Psychogeriatrics, 23, 512-522. [CrossRef] [PubMed] [Google Scholar]
- Reger, M.A., Henderson, S.T., Hale, C., Cholerton, B., Baker, L.D., Watson, G.S., Hyde, K., Chapman, D., Craft, S. (2004). Effects of β-hydroxybutyrate on cognition in memory-impaired adults. Neurobiol Aging, 25, 311-314. [CrossRef] [PubMed] [Google Scholar]
- Rojas-Morales, P., Pedraza-Chaverri, J., Tapia, E. (2020) Ketone bodies, stress response, and redox homeostasis. Redox Biol, 29, 101395. [CrossRef] [PubMed] [Google Scholar]
- Rusek, M., Pluta, R., Ułamek-Kozioł, M., Czuczwar, S.J. (2019). Ketogenic Diet in Alzheimer’s Disease. Int J Mol Sci, 20, 3892. [CrossRef] [PubMed] [Google Scholar]
- Ryu, J. C., Zimmer, E. R., Rosa-Neto, P., Yoon, S. O. (2019). Consequences of Metabolic Disruption in Alzheimer’s Disease Pathology. Neurotherapeutics, 16, 600-610. [CrossRef] [PubMed] [Google Scholar]
- Schönfeld, P., Wojtczak, L. (2016). Short- and medium-chain fatty acids in energy metabolism: The cellular perspective. J Lipid Res, 57, 943-954. [CrossRef] [PubMed] [Google Scholar]
- Shippy, D.C., Wilhelm, C., Viharkumar, P.A., Raife, T.J., Ulland, T.K. (2020) β-Hydroxybutyrate inhibits inflammasome activation to attenuate Alzheimer’s disease pathology. J Neuroinflammation, 17, 280. [Google Scholar]
- Simpson, I.A., Chundu, K.R., Davies-Hill, T., Honer, W.G., Davies, P. (1994). Decreased concentrations of GLUT1 and GLUT3 glucose transporters in the brains of patients with Alzheimer’s disease. Ann Neurol, 35, 546-551. [CrossRef] [PubMed] [Google Scholar]
- Sims, J.R., Zimmer, J.A., Evans, C.D., Lu, M., Ardayfio, P., Sparks, J., Wessels, A.M., Shcherbinin, S., Wang, H., Monkul Nery, E.S., Collins, E.C., Solomon, P., Salloway, S., Apostolova, L.G., Hansson, O., Ritchie, C., Brooks, D.A., Mintun, M., Skovronsky, D.M., TRAILBLAZER-ALZ 2 Investigators. (2023). Donanemab in Early Symptomatic Alzheimer Disease : The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA, e2313239. [Google Scholar]
- Soria Lopez, J.A., González, H.M., Léger, G.C. (2019). Alzheimer’s disease. Handb Clin Neurol, 167, 231-255. [CrossRef] [PubMed] [Google Scholar]
- Stampfer, M.J. (2006). Cardiovascular disease and Alzheimer’s disease: Common links. J Intern Med, 260, 211-223. [CrossRef] [PubMed] [Google Scholar]
- Stephen, R., Hongisto, K., Solomon, A., Lönnroos, E. (2017). Physical Activity and Alzheimer’s Disease: A Systematic Review. J Gerontol A Biol Sci Med Sci, 72, 733-739. [PubMed] [Google Scholar]
- Straus, D. S., Glass, C. K. (2007). Anti-inflammatory actions of PPAR ligands: New insights on cellular and molecular mechanisms. Trends Immunol, 28, 551-558. [CrossRef] [PubMed] [Google Scholar]
- Sumithran, P., Proietto, J. (2008). Ketogenic diets for weight loss: A review of their principles, safety and efficacy. Obes Res Clin Pract, 2, 1-13. [CrossRef] [Google Scholar]
- Swan, K., Hopper, M., Wenke, R., Jackson, C., Till, T., Conway, E. (2018). Speech-Language Pathologist Interventions for Communication in Moderate-Severe Dementia: A Systematic Review. Am J Speech Lang Pathol, 27, 836-852. [CrossRef] [MathSciNet] [Google Scholar]
- Taylor, M.K., Sullivan, D.K., Mahnken, J.D., Burns, J.M., Swerdlow, R.H. (2018). Feasibility and efficacy data from a ketogenic diet intervention in Alzheimer’s disease. Alzheimers Dement, 4, 28-36. [CrossRef] [Google Scholar]
- Terada, T., Obi, T., Bunai, T., Matsudaira, T., Yoshikawa, E., Ando, I., Futatsubashi, M., Tsukada, H., Ouchi, Y. (2020). In vivo mitochondrial and glycolytic impairments in patients with Alzheimer disease. Neurology, 94, e1592-e1604. [CrossRef] [PubMed] [Google Scholar]
- Turner, N., Hariharan, K., TidAng, J., Frangioudakis, G., Beale, S.M., Wright, L.E., Zeng, X.Y., Leslie, S.J., Li, J.-Y., Kraegen, E.W., Cooney, G.J., Ye, J.-M. (2009). Enhancement of Muscle Mitochondrial Oxidative Capacity and Alterations in Insulin Action Are Lipid Species Dependent. Diabetes, 58, 2547-2554. [CrossRef] [PubMed] [Google Scholar]
- Uemura, E., Greenlee, H.W. (2001). Amyloid β-Peptide Inhibits Neuronal Glucose Uptake by Preventing Exocytosis. Exp Neurol, 170, 270-276. [CrossRef] [PubMed] [Google Scholar]
- Volkmer, A., Rogalski, E., Henry, M., Taylor-Rubin, C., Ruggero, L., Khayum, R., Kindell, J., Gorno-Tempini, M.L., Warren, J.D., Rohrer, J.D. (2020). Speech and language therapy approaches to managing primary progressive aphasia. Pract Neurol, 20, 154-161. [CrossRef] [PubMed] [Google Scholar]
- Wang, Y., Liu, Z., Han, Y., Xu, J., Huang, W., Li, Z. (2018). Medium Chain Triglycerides enhances exercise endurance through the increased mitochondrial biogenesis and metabolism. PLoS ONE, 13, e0191182. [CrossRef] [PubMed] [Google Scholar]
- Wang, Y., Zhang, J., Zhang, Y., Yao, J. (2023). Bibliometric analysis of global research profile on ketogenic diet therapies in neurological diseases : Beneficial diet therapies deserve more attention. Front Endocrinol (Lausanne), 13, 1066785. [CrossRef] [PubMed] [Google Scholar]
- Wegmann, S., Biernat, J., Mandelkow, E. (2021). A current view on Tau protein phosphorylation in Alzheimer’s disease. Curr Opin Neurobiol, 69, 131-138. [CrossRef] [PubMed] [Google Scholar]
- Whitelock, E., Ensaff, H. (2018). On Your Own: Older Adults’ Food Choice and Dietary Habits. Nutrients, 10, 413. [CrossRef] [PubMed] [Google Scholar]
- Winkler, E.A., Nishida, Y., Sagare, A P., Rege, S.V., Bell, R.D., Perlmutter, D., Sengillo, J.D., Hillman, S., Kong, P., Nelson, A.R., Sullivan, J.S., Zhao, Z., Meiselman, H.J., Wenby, R.B., Soto, J., Abel, E.D., Makshanoff, J., Zuniga, E., De Vivo, D.C., Zlokovic, B.V. (2015). GLUT1 reductions exacerbate Alzheimer’s disease vasculo-neuronal dysfunction and degeneration. Nat Neurosci, 18, 521-530. [CrossRef] [PubMed] [Google Scholar]
- Wirrell, E., Eckert, S., Wong-Kisiel, L., Payne, E., Nickels, K. (2018). Ketogenic diet therapy in infants : Efficacy and tolerability. Pediatr Neurol, 82, 13-18 [CrossRef] [PubMed] [Google Scholar]
- Włodarek, D. (2019). Role of Ketogenic Diets in Neurodegenerative Diseases (Alzheimer’s Disease and Parkinson’s Disease). Nutrients, 11, 169. [CrossRef] [PubMed] [Google Scholar]
- Wu, Y., Chen, M., Jiang, J. (2019). Mitochondrial dysfunction in neurodegenerative diseases and drug targets via apoptotic signaling. Mitochondrion, 49, 35-45. [CrossRef] [PubMed] [Google Scholar]
- Xie, G., Tian, W., Wei, T., Liu, F. (2015). The neuroprotective effects of β-hydroxybutyrate on Aβ-injected rat hippocampus in vivo and in Aβ-treated PC-12 cells in vitro. Free Rad Res, 49, 139-150. [CrossRef] [PubMed] [Google Scholar]
- Xu, Y., Jiang, C., Wu, J., Liu, P., Deng, X., Zhang, Y., Peng, B., Zhu, Y. (2022). Ketogenic diet ameliorates cognitive impairment and neuroinflammation in a mouse model of Alzheimer’s disease. CNS Neurosci Ther, 28, 580-592. [Google Scholar]
- Yang, X., Cheng, B. (2010). Neuroprotective and Anti-inflammatory Activities of Ketogenic Diet on MPTP-induced Neurotoxicity. J Mol Neurosci, 42, 145-153. [CrossRef] [PubMed] [Google Scholar]
- Yin, F., Sancheti, H., Patil, I., Cadenas, E. (2016). Energy metabolism and inflammation in brain aging and Alzheimer’s disease. Free Radic Biol Med, 100, 108-122. [CrossRef] [PubMed] [Google Scholar]
- Youm, Y.-H., Nguyen, K.Y., Grant, R.W., Goldberg, E.L., Bodogai, M., Kim, D., D’Agostino, D., Planavsky, N., Lupfer, C., Kanneganti, T.D., Kang, S., Horvath, T.L., Fahmy, T.M., Crawford, P.A., Biragyn, A., Alnemri, E., Dixit, V.D. (2015). Ketone body β-hydroxybutyrate blocks the NLRP3 inflammasome-mediated inflammatory disease. Nat Med, 21, 263-269. [CrossRef] [PubMed] [Google Scholar]
- Yuan, X., Wang, J., Yang, S., Gao, M., Cao, L., Li, X., Hong, D., Tian, S., Sun, C. (2020). Effect of the ketogenic diet on glycemic control, insulin resistance, and lipid metabolism in patients with T2DM: A systematic review and meta-analysis. Nutr Diabetes, 10, 38. [CrossRef] [MathSciNet] [PubMed] [Google Scholar]
- Zandi-Nejad, K., Takakura, A., Jurewicz, M., Chandraker, A.K., Offermanns, S., Mount, D., Abdi, R. (2013). The role of HCA2 (GPR109A) in regulating macrophage function. FASEB J, 27, 4366-4374. [CrossRef] [PubMed] [Google Scholar]
- Zhang, C., Rissman, R. A., Feng, J. (2015). Characterization of ATP Alternations in an Alzheimer’s Disease Transgenic Mouse Model. J Alzheimers Dis, 44, 375-378. [CrossRef] [PubMed] [Google Scholar]
- Zhang, H., Wei, W., Zhao, M., Ma, L., Jiang, X., Pei, H., Cao, Y., Li, H. (2021). Interaction between Aβ and Tau in the Pathogenesis of Alzheimer’s Disease. Int J Biol Sci, 17, 2181-2192. [CrossRef] [PubMed] [Google Scholar]
- Zhong, N., Weisgraber, K. H. (2009). Understanding the Association of Apolipoprotein E4 with Alzheimer Disease: Clues from Its Structure. J Biol Chem, 284, 6027-6031. [CrossRef] [PubMed] [Google Scholar]
- Zhu, Y., Shan, X., Yuzwa, S.A., Vocadlo, D.J. (2014). The Emerging Link between O-GlcNAc and Alzheimer Disease. J Biol Chem, 289, 34472-34481. [CrossRef] [PubMed] [Google Scholar]
- Ziegler, D.R., Ribeiro, L.C., Hagenn, M., Siqueira, I.R., Araújo, E., Torres, I.L.S., Gottfried, C., Netto, C.A., Gonçalves, C.-A. (2003). Ketogenic diet increases glutathione peroxidase activity in rat hippocampus. Neurochem Res, 28, 1793-1797. [CrossRef] [PubMed] [Google Scholar]
Citation de l’article : Charlot, A., Lernould, A., Plus, I., et Zoll, J. (2023). Intérêt du régime cétogène dans la prise en charge de la maladie d’Alzheimer. Biologie Aujourd’hui, 217, 253-263
Liste des figures
 |
Figure 1 Stades d’évolution de la maladie d’Alzheimer. La maladie d’Alzheimer est progressive et se développe selon 4 stades : préclinique, prédémentiel, démentiel et démentiel évolué, où les symptômes de la maladie s’aggravent progressivement, jusqu’au décès du patient. |
| Dans le texte | |
 |
Figure 2 Mécanismes impliqués dans la neurodégénescence chez les patients atteints de la maladie d’Alzheimer. Au cœur des mécanismes de neurodégénerescence se trouvent les plaques amyloïdes, responsables de la mise en place d’un cercle vicieux, composé d’un hypométabolisme du glucose, de dysfonctions mitochondriales, d’une augmentation du stress oxydant et des processus inflammatoires, conduisant à un déficit énergétique. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
| Dans le texte | |
 |
Figure 3 Prise en charge globale des patients atteints de la maladie d’Alzheimer. La prise en charge de la maladie d’Alzheimer regroupe différents axes, notamment une approche médicamenteuse, un suivi psychologique, la mise en place d’activités physiques, ou encore un suivi orthophonique. Cette prise en charge pourrait également être renforcée par un encadrement nutritionnel. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
| Dans le texte | |
 |
Figure 4 Répartition des macronutriments de l’alimentation moderne versus l’alimentation cétogène. L’alimentation moderne est une alimentation où les glucides et les lipides occupent une part importante des macronutriments, alors que l’alimentation cétogène présente une restriction importante de la part des glucides et un enrichissement en lipides. |
| Dans le texte | |
 |
Figure 5 Utilisation des corps cétoniques comme substrat énergétique pour le cerveau. Les corps cétoniques sont produits par les mitochondries du foie à partir de l’Acétyl-CoA puis sécrétés dans la circulation sanguine. Ils sont ainsi transportés jusqu’au cerveau où ils sont transformés à nouveau en Acétyl-CoA, qui pourra entrer dans le cycle de Krebs pour produire de l’ATP. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
| Dans le texte | |
 |
Figure 6 Mécanismes de neuroprotection médiés par l’alimentation cétogène enrichie en MCT. L’alimentation cétogène enrichie en MCT permet de lutter contre l’hypométabolisme du glucose grâce à la production de corps cétoniques, qui assurent un apport suffisant en substrats énergétiques au cerveau. Elle permet aussi d’améliorer les capacités mitochondriales, de réduire le stress oxydant et l’inflammation, ce qui est également bénéfique pour protéger les capacités oxydatives mitochondriales. Figure réalisée en utilisant des images de Servier Medical Art. Servier Medical Art (Servier, Licence Creative Commons 3.0). |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.


