| Issue |
Biologie Aujourd’hui
Volume 217, Number 3-4, 2023
|
|
|---|---|---|
| Page(s) | 233 - 243 | |
| DOI | https://doi.org/10.1051/jbio/2023032 | |
| Published online | 29 novembre 2023 | |
Article
L’héritage épigénétique multigénérationnel chez l’Homme : le passé, le présent et les perspectives
Multigenerational epigenetic inheritance in human: the past, present and perspectives
Univ. Rennes, EHESP, Inserm, Irset (Institut de recherche en santé, environnement et travail) – UMR_S 1085, 9 avenue Léon Bernard, 35000 Rennes, France
* Auteur correspondant : Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Reçu :
1
Mai
2023
Résumé
De nos jours, de nombreuses études suggèrent que les programmes de développement de chaque individu seraient susceptibles d’être modifiés. Les changements phénotypiques acquis pourraient persister tout au long de la vie de l’individu et même être transmis à la génération suivante. Bien que le mécanisme exact de cette préservation ne soit pas encore bien compris, de nombreuses observations suggèrent que les altérations épigénétiques en réponse à l’influence des facteurs environnementaux seraient responsables de cette hérédité. Le nombre croissant de facteurs externes tels que le stress social, la pollution environnementale et les changements climatiques rend difficile l’adaptation à ce nouvel environnement. Selon la théorie de l’origine développementale des maladies humaines, formulée par David Barker, les conditions environnementales rencontrées au cours des premières phases du développement peuvent avoir des effets à long terme sur les phases ultérieures de la vie. Ce phénomène est lié à la plasticité biologique du développement, qui permet une reprogrammation des fonctions physiologiques en réponse à différents stimuli. L’exposition in utero à des polluants environnementaux accroîtrait la prédisposition à des pathologies survenant dans les phases précoces et tardives de la vie, non seulement pour les générations présentes mais aussi les suivantes. Nous avons résumé ici des résultats d’études épidémiologiques et épigénétiques menées ces dernières années sur des données humaines afin de savoir si les effets transgénérationnels observés dans des organismes modèles peuvent également exister chez l’homme.
Abstract
Nowadays, a growing body of evidence suggests that the developmental programs of each individual could be modified. The acquired new phenotypic changes could be persistent throughout the individual’s life and even transmitted to the next generation. While the exact mechanism for that preservation is not well understood yet, there are many evidences showing that epigenetic alterations, which are robust and dynamic in response to the influence of the environmental factors, could be responsible for that inheritance. A growing number of external factors such as social stress, environmental pollution and climate changes make adaptation to these environmental changes rather challenging. According to the Developmental Origin of Human Disease theory, formulated by David Barker, environmental conditions experienced during the first phases of development can have long term effects on later phases of life. This phenomenon is linked to the biological plasticity of development, which allows reprogramming of physiological functions in response to different stimuli. Consequently, in utero exposure to environmental pollutants can increase predisposition to different pathologies that can occur both in early and later phases of life not only in the living generation but also in subsequent ones. Here, we have summarised some findings in human epigenetic research studies performed for the past few years which address the question whether transgenerational effects observed in model organisms could also occur in humans.
Mots clés : épigénétique / héritage transgénérationnel / méthylation de l’ADN / facteurs environnementaux
Key words: epigenetics / transgenerational inheritance / DNA methylation / environmental factors
© Société de Biologie, 2023
Abréviations
3C : Capture conformationnelle du chromosome
5hmC : 5-hydroxyméthylcytosine
5mC : 5-méthyl-cytosine
AGPI n-3 : Acide gras polyinsaturé N-3
ARNnc : ARN non codant
ARNpi : ARN Piwi-interacting
BPA : Bisphénol A
CpG : Cytosine-phosphate-guanine
CSE : Cellules souches embryonnaires
H3K27me3 : Triméthylation de la lysine 27 de l’histone H3
H3K4me3 : Triméthylation de la lysine 4 de l’histone H3
PAI : Particules A intracisternales
PE : Perturbateurs endocriniens
PGC : Cellules germinales primordiales
Introduction
Le phénomène de l’héritage épigénétique transgénérationnel a fait l’objet d’une grande attention au cours des dernières décennies. Bien que les mécanismes de ce phénomène soient encore débattus, de nombreux chercheurs ont découvert que les organismes pouvaient s’adapter à un environnement changeant et que cette adaptation conduisait à l’acquisition de nouveaux traits phénotypiques qui pouvaient être détectés chez plusieurs générations suivantes. Bien que de nombreuses études aient été réalisées sur des organismes modèles, notamment la mouche, le nématode, la souris, le rat et le mouton, il existe des preuves que l’Homme pouvait également hériter de certaines caractéristiques induites par l’exposition de la génération précédente à certains facteurs environnementaux. La qualité des gamètes étant essentielle pour concevoir un enfant en bonne santé, la connaissance des risques potentiels de l’exposition à ces facteurs environnementaux pour les générations futures est un enjeu majeur de santé publique.
Définition de l’épigénétique
Les mécanismes épigénétiques sont conçus pour établir un phénotype sans modification de la séquence de l’ADN. Le terme « épigénétique » a été initialement proposé par Conrad Waddington. Une définition du concept de trait épigénétique en tant que « phénotype stable et héritable résultant de changements dans un chromosome sans altération de la séquence d’ADN » a été formulée lors d’une réunion à Cold Spring Harbor en 2008 (Berger et al., 2009). Des preuves de plus en plus nombreuses ont montré que la méthylation de l’ADN, les modifications des histones et les ARN non codants (ARNnc) sont susceptibles d’être altérés en raison de leur complexité et de leur régulation dynamique (Legoff et al., 2019). Les mécanismes épigénétiques régulent à leur tour de nombreuses fonctions cellulaires et processus de développement tout au long de la vie d’un individu.
Mécanismes épigénétiques
Le processus de différenciation cellulaire est un exemple de changement épigénétique. Au cours de la morphogenèse, les cellules souches totipotentes deviennent les différentes lignées de cellules pluripotentes de l’embryon, qui deviennent à leur tour des cellules entièrement différenciées sous l’action de processus épigénétiques. Ces mêmes processus sont également impliqués dans la régulation de l’empreinte, le « silençage » des gènes, l’inactivation du chromosome X, la reprogrammation de la méthylation de l’ADN, la progression de la cancérogenèse, la régulation des modifications des histones et de l’hétérochromatine (Legoff et al., 2019). Les mécanismes épigénétiques sont essentiels à l’établissement et au maintien de l’identité cellulaire. Bien que les marques épigénétiques soient relativement stables dans les cellules somatiques au cours de la vie adulte, l’épigénome est reprogrammé au cours du développement pour acquérir la totipotence. Les mécanismes épigénétiques pourraient notamment être affectés lors de la réparation de l’ADN. Lors de la réparation par recombinaison homologue d’une cassure double brin, les deux brins d’ADN réparés présentent des niveaux différents de cytosines méthylées (Figure 1). L’un des brins est fréquemment méthylé en aval de la rupture double brin réparée. L’autre brin d’ADN perd sa méthylation sur environ six sites CpG qui étaient auparavant méthylés en aval de la cassure double brin, ainsi que sur environ cinq sites CpG préalablement méthylés en amont de la cassure (Guozzo et al., 2007 ; Russo et al., 2016). Lorsque le chromosome est répliqué, il donne naissance à un premier chromosome fortement méthylé en aval du site de rupture précédent et à un second chromosome non méthylé dans la région située en amont et en aval de ce site. En ce qui concerne le gène rompu par la cassure double brin, la moitié des cellules de la descendance l’exprime à un niveau élevé alors que l’autre moitié voit son expression réprimée. Lorsque des clones de ces cellules sont maintenus en culture pendant trois ans, les nouveaux schémas de méthylation persistent pendant toute cette période.
L’héritage épigénétique transgénérationnel est la transmission de marqueurs et de modifications épigénétiques d’une génération à plusieurs générations suivantes sans altération de la structure primaire de l’ADN. Chez les mammifères, les gènes fortement méthylés dans le sperme sont rapidement déméthylés dans le zygote quelques heures seulement après la fécondation, avant le début du premier cycle de réplication de l’ADN (Oswald et al., 2000).
 |
Figure 1 Changements de méthylation de l’ADN à la suite de la recombinaison homologue. Les cassures double-brin induisent la méthylation de l’ADN si les cassures se produisent pendant la phase de synthèse de l’ADN et si elles sont réparées via un mécanisme de recombinaison homologue. |
Méthylation de l’ADN et établissement de cellules germinales
Les modifications de la méthylation de l’ADN sont essentielles à l’établissement des cellules germinales, car leur état épigénétique est préservé dans le sperme et affecte le développement embryonnaire. Chez les mammifères, la première reprogrammation de l’épigénome se produit au début du développement embryonnaire, du stade zygote à la formation des couches, et la seconde se produit pendant la transition entre la lignée somatique et la lignée germinale. Chez les mâles, un troisième événement se produit au cours de la spermatogenèse, lorsque l’histone est massivement remplacée par la protamine pour former des spermatozoïdes compacts. Cependant, la reprogrammation épigénétique rend problématique l’utilisation des patterns de méthylation de l’ADN comme moyen de transmission des effets induits sur le développement, car ces patterns sont réinitialisés à la fois dans la cellule germinale primordiale et dans l’embryon précoce (Seisenberger et al., 2012). L’héritage épigénétique doit donc être compatible avec la reprogrammation, un processus clé essentiel pour l’organogenèse et la production de cellules germinales. Pour donner naissance à un zygote totipotent capable de générer différents types de cellules dans le corps, tout programme épigénétique sexospécifique dans la lignée germinale doit être effacé. Cependant, des preuves récentes suggèrent que cet « effacement » pourrait ne pas être complet et qu’au moins une partie de la méthylation serait directement héritée. On a identifié 4730 loci qui échappent à la déméthylation dans les cellules germinales primordiales (PGC), et qui sont principalement associés à des répétitions (Hackett et al., 2013). Les loci résistants correspondent principalement à des particules A intracisternales (PAI). Les gènes « échappés » sont souvent adjacents à des éléments PAI ou à des régions télomériques (Hackett et al., 2013). Étant donné que de nombreux éléments régulateurs peuvent échapper à l’effacement de la 5-méthyl-cytosine (5mC) zygotique, des régions résistantes à la déméthylation, rares mais potentiellement pertinentes sur le plan fonctionnel, pourraient être héritées sur plusieurs générations en échappant à l’effacement lors de la reprogrammation zygotique et de la reprogrammation des PGC (Hackett et al., 2013). L’effacement de la méthylation CpG (pour donner la 5mC) dans les PGC se produit par conversion en 5-hydroxyméthylcytosine (5hmC), sous l’effet de niveaux élevés des TET (Ten-Eleven-Translocation) – méthyl-cytosine dioxygénases 1 et 2. L’inactivation des gènes Tet1 et Tet2 entraîne la régulation à la baisse d’un groupe de gènes comprenant ceux liés à la pluripotence, notamment Esrrb, Prdm14, Dppa3, Klf2, Tcl1 et Zfp42, ainsi qu’une augmentation de la méthylation de leurs promoteurs (Ficz et al., 2011). La diminution des niveaux de TET au cours de la différenciation a été associée à une diminution de l’ hydroxyméthylation au niveau des promoteurs des gènes spécifiques des cellules souches embryonnaires (CSE), ainsi qu’à une augmentation de la méthylation et de l’extinction des gènes (Ficz et al., 2011).
Modifications des histones et établissement de cellules germinales
Un autre mécanisme de préservation de la mémoire épigénétique pourrait impliquer les modifications des histones. Les marques d’histones sont importantes pour la structure de la chromatine, ainsi que pour l’accessibilité de facteurs de transcription aux domaines régulateurs et jouent un rôle important dans l’établissement de l’identité cellulaire. Une étude récente sur le zygote humain a montré que les gènes actifs, avec la marque de triméthylation de l’histone H3 de la lysine 4 (H3K4me3) dans les régions promotrices, sont essentiellement dépourvus de méthylation de leur ADN (Guo et al., 2014), suggérant que les marques H3K4me3 sont importantes pour la régulation de la méthylation de l’ADN au début du zygote. Les PGC précoces présentent également un niveau élevé de triméthylation de la lysine 27 de l’histone H3 (H3K27me3) en lien avec une forte activité d’EZH2, une enzyme du groupe polycomb. Les membres du complexe répresseur de polycomb, qui sont impliqués dans l’établissement des PGC, sont supposés être critiques pour l’héritage transgénérationnel. Notamment, la signature chromatinienne des cellules germinales est mise en place spécifiquement dans les PGC avant leur entrée dans les gonades, et est associée à l’expression élevée de gènes spécifiques de la pluripotence : Sox2, Oct4, Nanog et Stella 7 (Hajkova et al., 2008). L’analyse du génome entier des PGC au jour embryonnaire 11,5 a révélé des domaines bivalents H3K4me3/H3K27me3 fortement enrichis au niveau des gènes régulateurs du développement, d’une manière remarquablement similaire à celle des CSE. Les régulateurs du développement restent bivalents et transcriptionnellement silencieux jusqu’à l’initiation de la différenciation sexuelle au jour embryonnaire 13,5. Ces données démontrent l’existence de domaines bivalents dans la lignée germinale et suggèrent que le programme somatique soit continuellement maintenu comme bivalent, transmettant potentiellement un héritage épigénétique transgénérationnel (Sachs et al., 2013). Le rôle de H3K27me3 dans l’héritage transgénérationnel a également été démontré chez la mouche drosophile (Ciabrelli et al., 2017). La mémoire épigénétique pourrait ainsi être préservée par le maintien de l’occupation des histones au niveau des gènes essentiels de l’identité cellulaire. Une autre marque d’histone, H3K9me3, pourrait également jouer un rôle dans la transmission de l’héritage transgénérationnel. D’ailleurs, les changements induits par la température dans l’histone H3K9me3 peuvent persister pendant 14 générations chez le nématode C.elegans (Klosin et al., 2017).
Préservation de l’histone dans les spermatozoïdes
Les cellules germinales sont confrontées à un autre défi au cours de la spermatogenèse, lorsque l’histone est remplacée par la protamine pour acquérir la structure compacte. En fait, on sait depuis plus de 40 ans que les histones ne sont pas complètement remplacées par les protamines dans les spermatozoïdes, et on a postulé une fonction développementale spécifique pour la partie de la chromatine enrichie en histones (Gatewood et al., 1990). Cependant, l’existence d’une partie spécifique de la chromatine des spermatozoïdes qui serait constamment enrichie en histones n’a toujours pas été confirmée jusqu’à présent. Un récent profilage global des modifications des histones dans les spermatozoïdes humains et murins a indiqué que la fraction nucléosomale contient certains promoteurs du développement (Hammoud et al., 2009 ; Brykczynska et al., 2010). Bien que la question de savoir si les régions nucléosomiques des spermatozoïdes sont des régions pauvres en gènes ou des promoteurs soit encore débattue, il a pu être confirmé qu’une fraction du génome contient des histones. Les marques d’histones pourraient donc être stratégiquement déployées pour propager l’information épigénétique à travers les générations. Les tests d’immunoprécipitation et de séquençage de la chromatine, qui permettent d’obtenir des données fiables à partir d’un nombre limité de cellules à des stades embryonnaires précoces, jettent un nouvel éclairage sur le devenir des histones parentales. Lors de la fécondation, les marques d’histones H3K4me3 sont largement épuisées dans les zygotes et ne sont observées qu’après l’activation majeure du génome zygotique à la fin du stade de deux cellules. Une petite quantité de H3K4me3 paternelle est présente dans les zygotes, ce qui suggère que ces marques resteraient disponibles dans certains promoteurs pour une activation tardive et qu’elles transmettraient une mémoire épigénétique paternelle (Zhang et al., 2016).
La question de savoir si des traits comportementaux acquis peuvent être transmis d’une génération à la suivante fait encore l’objet de débats. Dans ce cadre, l’observation rapportée récemment par Rosenberg et al. (2022) chez le poulet présente un intérêt tout particulier. Ces auteurs ont rapporté que le chauffage d’embryons de poussins de première génération a induit des réponses thermiques et immunologiques également détectées dans des générations non directement soumises à ce traitement. L’analyse transcriptomique a confirmé que le conditionnement embryonnaire par la chaleur induit des changements dans l’expression des gènes au niveau de l’hypothalamus, induisant ces phénotypes dans leur descendance. Rosenberg et al. (2022) ont proposé que l’un des mécanismes sous-jacents à l’héritage transgénérationnel puisse dépendre de la réorganisation tridimensionnelle de la chromatine. Le test 3C a confirmé que les interactions les plus fortes intervenaient entre l’enhancer de HSP25 et le promoteur de SOCS3 situés à distance. La réorganisation de la chromatine tridimensionnelle pourrait donc être l’un des mécanismes de l’hérédité transgénérationnelle de traits acquis.
Modifications de la méthylation de l’ADN et hérédité transgénérationnelle
On estime que ∼70 % de l’ADN dans le sperme de souris et humain est dans un état méthylé (Molaro et al., 2011). Cette méthylation élevée de l’ADN dans les spermatozoïdes est essentielle pour la fertilité et la viabilité de la progéniture (Okano et al., 1999 ; Bourc’his & Bestor, 2004). Des modifications de la méthylation de l’ADN comme mécanisme épigénétique possible médiateur de l’héritage transgénérationnel de traits acquis ont été mises en évidence chez plusieurs espèces, dont le mouton (Braz et al., 2022), la souris (Lane et al., 2003 ; Guerrero-Bosagna et al., 2012 ; Pépin et al., 2022) et le rat (Anway et al., 2005 ; Ben Maamar et al., 2021) (Figure 2).
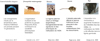 |
Figure 2 Quelques preuves d’hérédité épigénétique transgénérationnelle dans des organismes modèles. |
Modifications des histones et hérédité transgénérationnelle
Le rôle des modifications des histones dans l’hérédité transgénérationnelle est moins étudié. Il est important de noter que l’hérédité transgénérationnelle est médiée par des altérations dans des régions limitées du génome, y compris les régulateurs principaux des gènes de la pluripotence (Hao et al., 2016 ; Gély-Pernot et al., 2018). Par exemple, des changements dans H3K4me3 ont été détectés au niveau du promoteur du gène Pou5f1/Oct4 dans les testicules de souris mâles des générations F1 et F3 issues de femelles ayant été exposées au cours de la gestation (F0) à l’atrazine, un herbicide largement utilisé dans des cultures de maïs, sorgho et canne à sucre. Le facteur de pluripotence Pou5f1/Oct4 régule environ 500 gènes. Ainsi, les changements dans les gènes régulateurs maîtres pourraient avoir des effets qui vont bien au- delà de ces gènes en raison de l’existence d’un vaste réseau transcriptionnel. Cependant, la grande majorité des marques d’histones n’est pas héritée, ce qui suggère que seule une fraction limitée du génome peut résister aux événements de reprogrammation. Quoi qu’il en soit, l’exemple de l’exposition prénatale à l’atrazine montre que les changements d’expression génétique liés à des modifications d’histones au niveau de promoteurs peuvent être conservés sur (au moins) trois générations (Hao et al., 2016).
Un autre exemple est celui de l’exposition prénatale au bisphénol A (BPA), au bisphénol E (BPE) et au bisphénol S (BPS) au cours de la gestation, toujours chez la souris (Shi et al., 2019). Ce traitement induit des effets transgénérationnels sur les fonctions reproductives masculines, probablement en raison d’une modification épigénétique consécutive à la perturbation des DNA méthyl-transférases et des marques d’histones dans le testicule néonatal et/ou adulte (Shi et al., 2019). L’analyse du sperme des mâles transgéniques KDM1A a révélé l’existence de nombreuses régions présentant un enrichissement H3K4me3 altéré sur l’allèle paternel de l’embryon préimplantatoire. Une altération de la triméthylation de l’histone H3 de la lysine 4 dans le sperme a été également rapportée à propos de l’hérédité épigénétique transgénérationnelle de troubles métaboliques associés à l’obésité induite par un régime riche en graisses chez la souris mâle F0 (Pépin et al., 2022). Ces résultats confirment que l’histone méthylée H3K4me3 du sperme joue un rôle dans la transmission des changements phénotypiques par le biais de mécanismes épigénétiques (Lismer et al., 2020).
ARN non codants dans l’hérédité transgénérationnelle
Un autre mécanisme épigénétique impliqué dans l’hérédité transgénérationnelle est la régulation par les ARNnc, qui sont des ARN fonctionnels non traduits en protéines. Les ARNnc sont impliqués dans de multiples processus cellulaires. L’expression de nombreux gènes est régulée par les ARNnc. L’expression de la majorité des ARNnc est spécifique d’un tissu donné. L’ARNnc joue un rôle dans l’héritage épigénétique transgénérationnel. La composition de l’ARNnc dans les spermatozoïdes a été analysée par séquençage de l’ARN de spermatozoïdes immatures et matures situés dans différentes régions de l’épididyme. Les analyses ont montré que la composition en ARNnc des spermatozoïdes changeait considérablement, avec à la fois une perte et une acquisition de différents ARNnc, principalement dans la partie distale de l’épididyme (Nixon et al., 2015). Une autre étude a suivi l’évolution de la composition des ARNnc lors du passage des spermatocytes pachytènes aux spermatozoïdes immatures, et des spermatozoïdes caput aux spermatozoïdes cauda de l’épididyme. Elle a montré que l’ARNnc prédominant dans les testicules est l’ARN Piwi-interacting (l’ARNpi) et que le transfert dans l’épididyme est associé à une perte de presque tous les ARNpi et à une augmentation remarquable des fragments d’ARNt (Sharma et al., 2018). L’ARNm Let-7c, qui est régulé à la hausse dans le sperme de souris mâles nourries avec un régime riche en graisses, l’est également dans le tissu adipeux de leur progéniture F1. Cet ARNm est connu pour réguler l’homéostasie du glucose et la sensibilité à l’insuline et a été associé à une prédisposition au diabète de type 2. L’importance de l’ARNnc dans la transmission paternelle de l’obésité et du diabète a également été confirmée par une expérience au cours de laquelle des ARNnc ont été injectés dans des zygotes : l’injection de l’ARNnc du sperme d’une souris mâle nourrie avec un régime riche en graisses dans un zygote témoin a entraîné des troubles métaboliques chez la progéniture, tandis que l’injection de l’ARNnc du sperme d’un mâle nourri avec un régime contrôle n’a pas eu d’effet (Grandjean et al., 2015). Par ailleurs, l’exposition paternelle au phtalate de dicyclohéxyle, un perturbateur endocrinien très présent dans les plastiques, a entraîné une résistance exacerbée à l’insuline et une altération de la signalisation de l’insuline chez la progéniture F1 sans affecter l’obésité induite par l’alimentation. Cette même exposition paternelle peut également avoir des effets négatifs transgénérationnels spécifiques au sexe chez la descendance F2 et provoquer une intolérance au glucose chez la descendance F2 femelle (Liu et al., 2023). Ainsi, ces études chez la souris permettent de conclure que la composition de l’ARNnc du sperme est très sensible au stress environnemental, et que les changements induits dans ces conditions peuvent avoir des effets à long terme sur l’expression des gènes dans différents tissus (Figure 3).
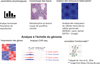 |
Figure 3 Analyse phénotypique et épigénétique dans les études transgénérationnelles. Pour l’analyse des effets induits par des facteurs exogènes, plusieurs paramètres sont pris en compte ; par exemple, l’analyse de coupes de tissus colorées à l’hématoxyline-éosine peut révéler des changements morphologiques. Des marqueurs spécifiques aideront à identifier plus finement d’éventuels changements dans les cellules. Enfin, en utilisant la technique des ‘omiques’, on peut analyser les changements à l’échelle génomique. Cette dernière approche a notamment permis de révéler de nouveaux biomarqueurs des effets de l’atrazine (Hao et al., 2016). L’analyse (par CHIP-seq) a montré une augmentation des marques H3K4me3 au niveau du promoteur du gène Pou5f1 dans les testicules mâles F1 et F3 suite à l’exposition prénatale à l’herbicide atrazine. |
Effets épigénétiques multigénérationnels chez l’homme
La plupart des expériences sur l’hérédité transgénérationnelle a été réalisée sur des organismes modèles de rongeurs. La question de savoir si les effets observés sont similaires chez l’Homme est débattue. Premièrement, dans les expériences sur les modèles animaux, les chercheurs utilisent très souvent des doses élevées de substances toxiques, ce qui n’est pas le cas pour l’exposition humaine. Deuxièmement, la durée de vie des animaux modèles étant plus courte, il n’est pas évident que les changements observés chez les rongeurs puissent persister pendant la longue durée de vie de l’humain. Troisièmement, il existe des différences dans le programme de développement des cellules germinales entre la souris et l’Homme, de sorte qu’il n’est pas certain que les cellules germinales humaines puissent conserver des informations épigénétiques similaires à celles des rongeurs. Néanmoins, de nombreux éléments étayent l’hypothèse selon laquelle une transmission épigénétique d’une génération à l’autre pourrait également exister chez l’Homme.
Certaines études montrent en particulier que les stimuli externes du développement précoce chez l’Homme peuvent avoir un effet sur la vie adulte. Il n’est toutefois pas certain que les changements induits par ces événements précoces puissent être transmis aux générations suivantes. La persistance d’altérations phénotypiques en l’absence de stimuli externes chez la descendance non exposée pourrait laisser à penser que certaines altérations puissent être fixées au niveau épigénétique. Pour être transmis aux générations suivantes, certains changements épigénétiques pourraient avoir lieu au niveau des cellules germinales. Ainsi, l’étude de l’épigénétique des cellules germinales devrait répondre à la question de l’héritage transgénérationnel.
Les exemples d’études humaines rapportés dans les sections suivantes ne sont pas encore véritablement des exemples d’études transgénérationnelles mais plutôt des preuves de la persistance de changements phénotypiques d’une génération à l’autre. Les changements épigénétiques pourraient être à l’origine de l’acquisition d’un nouveau phénotype. Par rapport aux modifications génétiques, les modifications épigénétiques sont moins aléatoires et plus robustes et peuvent être reproduites à chaque division cellulaire. La réponse définitive à la question de savoir si les effets induits pourraient être héréditaires nécessiterait des études montrant la transmission effectuée au niveau des cellules germinales.
Études sur la famine et les préférences alimentaires
Les premières données en faveur de l’hérédité transgénérationnelle d’un phénotype acquis chez l’Homme proviennent d’études historiques sur la famine. Un exemple bien connu est celui de la famine aiguë aux Pays-Bas. Au cours des derniers mois de la Seconde Guerre mondiale, les régions occidentales des Pays-Bas ont été touchées par une famine sévère, également connue sous le nom d’hiver de la faim. L’apport alimentaire, toutes sources confondues, a été réduit à des niveaux extrêmement bas. La faim a contribué à l’augmentation de la mortalité due aux maladies infectieuses et aux maladies du système digestif. Plusieurs études de suivi portant sur des populations sélectionnées ont permis d’analyser plus particulièrement les conséquences à long terme, toutes délétères, de la famine sur les résultats reproductifs des femmes ayant accouché pendant l’hiver de la faim, sur le poids à la naissance, les malformations et la mortalité périnatale des nouveau-nés exposés à la famine pendant la gestation, et sur la situation médicale et psychologique des enfants nés pendant la famine (Lumey & Van Poppel, 1994). Par ailleurs, une autre étude a montré que les enfants de pères sous-alimentés pendant la période prénatale, mais pas les mères, étaient plus lourds et plus obèses que les enfants de pères et de mères qui n’avaient pas été sous-alimentés pendant cette période (Veenendaal et al., 2013). Enfin, Van Abeelen et al. (2011) ont apporté la preuve directe que les changements dans le régime alimentaire de la mère pendant la grossesse modifient la relation entre la taille du placenta et l’hypertension ultérieure dans la descendance masculine, mais pas féminine.
Plusieurs études sur la famine en Chine ont fourni d’autres preuves de ses effets chez l’Homme. Par exemple, il a été montré qu’une grave carence nutritionnelle au début de la vie peut augmenter le risque de cancer de l’estomac à un stade ultérieur de l’existence (Li et al., 2012) et accroître le risque de diabète de type 2 à l’âge adulte, en particulier chez les femmes (Wang et al., 2016). L’exposition à la famine pendant les premières années de la vie augmente le risque d’anémie à l’âge adulte (Shi et al., 2013). De plus, la famine augmente le risque de symptômes neurologiques tels que l’altération des fonctions cognitives, des capacités visuomotrices, de la flexibilité mentale et de l’attention sélective à l’âge adulte (Li et al., 2015). Ces effets de la famine ont été observés chez deux générations consécutives d’adultes (Li et al., 2017).
Les conséquences de modifications du régime alimentaire ont été également analysées au niveau de l’épigénome. Ainsi, Daniels et al. (2020) ont montré qu’un apport calorique élevé en glucides pendant la grossesse pouvait moduler la méthylation de l’ADN du gène de la leptine dans le placenta. La mise en évidence d’une faible méthylation de l’ADN peut indiquer que le placenta répond à un apport calorique élevé en augmentant le niveau d’expression de cette hormone au cours du développement fœtal (Daniels et al., 2020). Des études d’association à l’échelle de l’épigénome, menées dans une population arabe, ont révélé des associations significatives entre le diabète de type 2, un IMC élevé et des méthylations dans les gènes DQX1, SOCS3, SBNO2, PRR5L et TXNIP (Al Muftah et al., 2016). Dans une autre étude, un complément alimentaire, l’acide gras polyinsaturé N-3 (AGPI n-3), qui n’est pas produit de manière endogène chez l’Homme, a été inclus dans le régime alimentaire. Les molécules d’AGPI n-3 sont essentielles au développement neuronal et contribuent à réduire le risque de maladies cardio-métaboliques. L’existence d’une association entre les apports maternels en AGPI n-3 et la méthylation de l’ADN de la progéniture a été démontrée dans les cellules mononucléaires du sang du cordon ombilical (Bianchi et al., 2019).
Facteurs de stress
Les enfants exposés in utero à des niveaux élevés de stress objectif ont des fonctions cognitives altérées. En janvier 1998, la province canadienne du Québec a connu une crise due à une tempête de verglas. Les enfants dont la mère avait subi un stress prénatal pendant cette période avaient un QI complet, un QI verbal et des capacités linguistiques inférieurs à ceux des enfants exposés à des niveaux faibles ou modérés de stress maternel prénatal objectif (Laplante et al., 2008). Khashan et al. (2011) ont également rapporté des données montrant que l’exposition maternelle prénatale à des événements de vie graves peut augmenter le risque de troubles affectifs chez la progéniture masculine. D’une manière générale, il est bien établi que l’exposition prénatale à une catastrophe naturelle modérément sévère est associée à des capacités cognitives et langagières plus faibles chez les enfants de 5 ans et demi. Lorsque le stress prénatal est causé par un état de guerre, les conséquences pour le nouveau-né sont associées à la méthylation de l’ADN au niveau du récepteur des glucocorticoïdes NR3C1 (Rodney & Mulligan, 2014).
Le tabagisme
Le tabagisme est un autre facteur de risque important pour le développement humain. L’étude ALSPAC (Avon Longitudinal Study of Parents and Children) a montré que les fils de pères ayant commencé à fumer régulièrement avant la puberté (< 13 ans) avaient une masse grasse plus importante pendant l’enfance, l’adolescence et le début de l’âge adulte (Golding et al., 2022). En outre, si le grand-père paternel avait commencé à fumer avant la puberté, ses petites-filles, mais pas ses petits-fils, présentaient des signes d’excès de masse grasse à deux âges : à 17 ans et à 24 ans. Bien plus, lorsque les pères des grands-pères maternels avaient commencé à fumer avant la puberté, leurs arrière-petites-filles, mais pas leurs arrière-petits-fils, présentaient un excès de masse grasse à ces mêmes âges. Une analyse de sensibilité n’a pas révélé d’association similaire avec la masse maigre. Cette étude de Golding et al. (2022) est la première à démontrer les effets transgénérationnels d’une exposition environnementale sur quatre générations. Une autre méta-analyse portant sur 13 cohortes (n = 6685) a montré qu’il existe une forte association entre le tabagisme maternel pendant la grossesse et la méthylation de l’ADN dans le sang du nouveau-né. En l’occurrence, Joubert et al. (2016) ont pu identifier à l’échelle du génome 6000 CpG différentiellement méthylés en relation avec le tabagisme maternel (Joubert et al., 2016).
Composés perturbateurs endocriniens
Un grand nombre de composés chimiques, dont on sait ou dont on pense qu’ils perturbent la signalisation endocrinienne, et appelés perturbateurs endocriniens (PE), sont connus. Ces composés sont omniprésents dans l’environnement puisqu’ils sont des composants majeurs de nombreux produits industriels et pesticides et sont présents dans des produits d’usage courant, tels que les aliments, les matériaux d’emballage alimentaire et les cosmétiques. Le BPA est l’un des PE les mieux étudiés. Des études ont montré que l’exposition maternelle au BPA pouvait modifier la méthylation de l’ADN au niveau du gène BDNF, essentiel au développement du cerveau, chez les adolescents (Mustieles et al., 2022). Bien plus, toujours à la suite d’une l’exposition maternelle au BPA, une augmentation de l’occupation de l’histone triméthylée H3K4me3 a été observée au niveau des promoteurs des gènes codant pour les histones acétyltransférases, les facteurs de liaison à l’ADN télomérique et les gènes de réparation de l’ADN (D’Cruz et al., 2022). Une étude sur le cordon ombilical humain exposé cette fois au composé œstrogénique chlordécone a mis en évidence une altération de la distribution de cette même histone H3K4me3 à l’échelle du génome dans les gènes liés à la ségrégation des chromosomes, à l’organisation de la chromatine et au cycle cellulaire (Legoff et al., 2021).
Bien qu’il n’y ait aucune preuve que les PE puissent causer des effets transgénérationnels chez l’homme, les études animales ont montré que les altérations hormonales pouvaient affecter le développement des cellules germinales et donc avoir des effets transgénérationnels. Les études confirmant les effets transgénérationnels induits par les PE chez l’animal concernent en particulier l’exposition au BPA et à des composés antiandrogéniques comme la vinclosoline et l’atrazine.
Pollution atmosphérique et contaminants environnementaux
Les particules atmosphériques, qui augmentent chaque année dans le monde entier, constituent une autre forme de pollution qui alerte l’opinion publique mondiale. En raison de leur très petite taille, les particules gagnent facilement le flux sanguin et sont distribuées à chaque organe par la circulation. Les particules peuvent adsorber à leur surface les métaux lourds, les pesticides et d’autres composés présents dans l’air. L’exposition à la pollution atmosphérique pendant la grossesse pourrait être associée à des troubles neurologiques tels que le trouble déficitaire de l’attention avec hyperactivité. En lien avec ce risque clinique, l’analyse de l’épigénome a montré que la méthylation de l’ADN était perturbée dans les gènes impliqués dans l’importante voie de signalisation Notch, qui est essentielle au développement du système nerveux (Feil et al., 2023).
D’autres composés présents dans la nature, comme l’arsenic, peuvent affecter plusieurs générations chez l’Homme. Une étude familiale portant sur trois générations, dans laquelle chaque génération vivant dans le même foyer a été exposée à l’arsenic à des moments différents : à l’âge adulte, in utero et pendant la petite enfance, a montré des changements détectables dans la méthylation de l’ADN au niveau de la lignée germinale même si l’exposition avait eu lieu plusieurs décennies avant l’analyse épigénétique. Les changements les plus significatifs dans la méthylation globale de l’ADN ont été observés chez les sujets souffrant de lésions cutanées dues à l’arsenic. L’exposition d’une génération à l’autre a permis de partager des loci et des régions d’ADN différentiellement méthylés (744 DML et 15 DMR) malgré le moment différent de l’exposition dans chaque génération. Six gènes ont été les plus significativement altérés : MLKL, VIPR2, ACY3 et SLC16A3 (Guo et al., 2018).
Remarques finales
En raison de questions éthiques et de la disponibilité limitée de matériel embryonnaire humain, les études de transmission épigénétique transgénérationnelle chez l’Homme sont problématiques. Sur la base des changements phénotypiques observés, quelques analyses limitées sur des spécimens humains ont cependant pu être réalisées. Une question fondamentale se dégage des études épidémiologiques humaines : (1) les changements morphologiques acquis associés à certaines modifications épigénétiques dans le sang périphérique peuvent-ils refléter ce qui s’est passé dans les cellules germinales ? ; (2) et même si des modifications épigénétiques sont détectées dans les cellules germinales telles que les spermatozoïdes, seront-elles préservées dans le zygote après la fécondation ? Étant donné qu’entre la première et la troisième génération, plusieurs reprogrammations ont lieu, on ne sait pas exactement dans quelle mesure les changements induits dans les spermatozoïdes résisteraient à la reprogrammation et se transmettraient à la génération suivante. Les mécanismes qui sous-tendent l’héritage transgénérationnel chez l’Homme devraient pouvoir être découverts à l’avenir grâce au développement de nouvelles technologies. Le séquençage de l’ARN et de l’ADN d’une seule cellule et le protocole de séquençage ChIP-seq sur une quantité limitée de matériel, ainsi que l’essai de capture conformationnelle des chromosomes et la microscopie à ultra-haute résolution ouvrent de nouvelles perspectives dans ce domaine. L’analyse des métadonnées de différentes cohortes, y compris les programmes européens HBM4EU et PARC, ouvre de nouvelles perspectives pour cette recherche (Encadré 1).
Comment étudier les changements épigénétiques ?
Analyse de la méthylation de l’ADN. Elle peut être effectuée sur des échantillons humains tels que le sang, les spermatozoïdes, le placenta et le cordon ombilical. L’analyse comprend l’extraction de l’ADN et : 1) l’analyse ciblée de la méthylation de l’ADN par conversion au bisulfite et pyroséquençage ; 2) l’analyse de la méthylation de l’ADN à l’aide de matrices d’hybridation de séquences humaines méthylées connues (cette méthode basée sur l’hybridation est la plus couramment utilisée dans les études épidémiologiques humaines) ; 3) l’enrichissement de l’ADN méthylé avec un anticorps ou une protéine de liaison de l’ADN méthylé, suivi d’un séquençage à l’échelle du génome à l’aide de la technologie Illumina ; 4) le séquençage à l’échelle du génome de l’ADN converti au bisulfite à l’aide de la technologie Illumina.
Analyse de l’occupation des régions de génome par modifications des histones. La méthode repose sur l’immunoprécipitation de la chromatine suivie du séquençage du génome. La méthode nécessite un anticorps de qualité ChIP et des tissus bien conservés avant l’analyse.
Analyse des modifications des histones du génome par immunofluorescence. Cette méthode repose sur la préparation de tissus inclus en paraffine et sur l’incubation des coupes de tissus avec un anticorps spécifique, suivie d’une détection fluorescente du signal. Cette méthode ne permet que d’estimer les niveaux globaux d’histones modifiées.
Analyse de l’ARN non codant. L’ARN non codant peut être analysé par l’extraction de petits ou longs ARN non codants, la construction d’une bibliothèque suivie d’un séquençage à l’aide de la technologie Illumina.
Remerciements
Ce travail a été soutenu par le programme national de recherche « Environnement-Santé-Travail » de l’ANSES (Projet R20155NN).
Références
- Al Muftah, W.A., Al-Shafai, M., Zaghlool, S.B., Visconti, A., Tsai, P.C., Kumar, P., Spector, T., Bell, J., Falchi, M., Suhre, K. (2016). Epigenetic associations of type 2 diabetes and BMI in an Arab population. Clin Epigenet, 8, 13. [CrossRef] [PubMed] [Google Scholar]
- Anway, M.D., Cupp, A.S., Uzumcu, M., Skinner, M.K. (2005). Epigenetic transgenerational actions of endocrine disruptors and male fertility. Science, 308, 1466-1469. [CrossRef] [PubMed] [Google Scholar]
- Ben Maamar, M., Beck, D., Nilsson, E.E., Kubsad, D., Skinner, M.K. (2021). Epigenome-wide association study for glyphosate induced transgenerational sperm DNA methylation and histone retention epigenetic biomarkers for disease. Epigenetics, 16, 1150-1167. [CrossRef] [PubMed] [Google Scholar]
- Berger, S.L., Kouzarides, T., Shiekhattar, R., Shilatifard, A. (2009). An operational definition of epigenetics. Genes Dev, 23, 781-783. [CrossRef] [PubMed] [Google Scholar]
- Bianchi, M., Alisi, A., Fabrizi, M., Vallone, C., Ravà, L., Giannico, R., Vernocchi, P., Signore, F., Manco, M. (2019). Maternal intake of N-3 polyunsaturated fatty acids during pregnancy is associated with differential methylation profiles in cord blood white cells. Front Genetics, 10, 1050. [CrossRef] [Google Scholar]
- Bourc’his, D., Bestor, T.H. (2004). Meiotic catastrophe and retrotransposon reactivation in male germ cells lacking Dnmt3L. Nature, 431, 96-99. [CrossRef] [PubMed] [Google Scholar]
- Braz, C.U., Taylor, T., Namous, H., Townsend, J., Crenshaw, T., Khatib, H. (2022). Paternal diet induces transgenerational epigenetic inheritance of DNA methylation signatures and phenotypes in sheep model. PNAS Nexus, 1(2), pgac040. [CrossRef] [Google Scholar]
- Brykczynska, U., Hisano, M., Erkek, S., Ramos, L., Oakeley, E.J., Roloff, T.C., Beisel, C., Schübeler, D., Stadler, M.B., Peters, A.H.F.M. (2010). Repressive and active histone methylation mark distinct promoters in human and mouse spermatozoa. Nature, Struct Mol Biol, 17, 679-687. [CrossRef] [PubMed] [Google Scholar]
- Ciabrelli, F., Comoglio, F., Fellous, S., Bonev, B., Ninova, M., Szabo, Q., Xuéreb, A., Klopp, C., Aravin, A., Paro, R., Bantignies, F., Cavalli, G (2017). Stable polycomb-dependent transgenerational inheritance of chromatin states in drosophila. Nature Genet, 49, 876-886. [CrossRef] [PubMed] [Google Scholar]
- Guozzo, C., Porcellini, A., Angrisano, T., Morano, A., Lee, B., Di Pardo, A., Messina, S., Iuliano, R., Fusco, A., Santillo, M.R., Muller, M.T., Chiariotti, L., Gottesman, M.E., Avvedimento, E.V. (2007). DNA damage, homology-directed repair, and DNA methylation. PLoS Genet, 3, e110. [CrossRef] [PubMed] [Google Scholar]
- Daniels, T.E., Sadovnikoff, A.I., Ridout, K.K., Lesseur, C., Marsit, C.J., Tyrka, A.R. (2020). Associations of maternal diet and placenta leptin methylation. Mol Cell Endocrinol, 505, 110739. [CrossRef] [PubMed] [Google Scholar]
- D’Cruz, S.C., Hao, C., Labussiere, M., Mustieles, V., Freire, C., Legoff, L., Magnaghi-Jaulin, L., Olivas-Martinez, A., Rodriguez-Carrillo, A., Jaulin, C., David, A., Fernandez, M. F., Smagulova, F. (2022). Genome-wide distribution of histone trimethylation reveals a global impact of bisphenol A on telomeric binding proteins and histone acetyltransferase factors: A pilot Study with Human and in Vitro Data. Clin Epigenet, 14, 186. [CrossRef] [PubMed] [Google Scholar]
- Feil, D., Abrishamcar, S., Christensen, G.M., Vanker, A., Koen, N., Kilanowski, A., Hoffman, N., Wedderburn C.J., Donald, K.A., Kobor M.S., Zar, H.J., Stein, D.J., Hüls A. (2023). DNA methylation as a potential mediator of the association between indoor air pollution and neurodevelopmental delay in a South African birth cohort. Clin Epigenet, 15, 31. [CrossRef] [Google Scholar]
- Ficz, G., Branco, M.R., Seisenberger, S., Santos, F., Krueger, F., Hore, T.A., Marques, C.J., Andrews, S., Reik, W. (2011). Dynamic regulation of 5-Hydroxymethylcytosine in mouse ES cells and during differentiation. Nature, 473, 398-402. [CrossRef] [PubMed] [Google Scholar]
- Gatewood, J.M., Cook, G.R., Balhorn, R., Schmid, C.W., Bradbury, E.M. (1990). Isolation of four core histones from human sperm chromatin representing a minor subset of somatic histones. J Biol Chem, 265, 20662-20666. [CrossRef] [PubMed] [Google Scholar]
- Gély-Pernot, A., Hao, C., Legoff, L., Multigner, L., D’Cruz, S.C., Kervarrec, C., Jégou, B., Tevosian, S., Smagulova, F. (2018). Gestational exposure to chlordecone promotes transgenerational changes in the murine reproductive system of males. Sci Rep, 8, 10274. [CrossRef] [PubMed] [Google Scholar]
- Golding, J., Gregory, S., Northstone, K., Pembrey, M., Watkins, S., Iles-Caven, Y., Suderman, M. (2022). Human transgenerational observations of regular smoking before puberty on fat mass in grandchildren and great-grandchildren. Sci Rep, 12, 1139. [CrossRef] [PubMed] [Google Scholar]
- Grandjean, V., Fourré, S., Fernandes De Abreu, D.A., Derieppe, M.A., Rémy, J.J., Rassoulzadegan, M. (2015). RNA-mediated paternal heredity of diet-induced obesity and metabolic disorders. Sci Rep, 5, 18193. [CrossRef] [PubMed] [Google Scholar]
- Guerrero-Bosagna, C., Covert, T.R., Haque, M.M., Settles, M., Nilsson, E.E., Anway, M.D., Skinner, M.K. (2012). Epigenetic transgenerational inheritance of vinclozolin induced mouse adult onset disease and associated sperm epigenome biomarkers. Reprod Toxicol, 34, 694-707. [CrossRef] [PubMed] [Google Scholar]
- Guo, H., Zhu, P., Yan, L., Li, R., Hu, B., Lian, Y., Yan, J., Ren, X., Lin, S., Li, J., Jin, X., Shi, X., Liu, P., Wang, X., Wang, W., Wei, Y., Li, X., Guo, F., Wu, X., Fan, X., Yong, J., Wen, L., Xie, S. X., Tang, F., Qiao, J. (2014). The DNA methylation landscape of human early embryos. Nature, 511, 606-610. [CrossRef] [PubMed] [Google Scholar]
- Guo, X., Chen, X., Wang, J., Liu, Z., Gaile, D., Wu, H, Yu, G., Mao, G., Yang, Z., Di, Z., Guo, X., Cao, L., Chang, P., Kang, B., Chen, J., Gao, W., Ren, X. (2018). Multi-generational impacts of arsenic exposure on genome-wide DNA methylation and the implications for arsenic-induced skin lesions. Environ Int, 119, 250-263. [CrossRef] [PubMed] [Google Scholar]
- Hackett, J.A., Sengupta, R., Zylicz, J.J., Murakami, K., Lee, C., Down, T.A., Surani, M.A. (2013). Germline DNA demethylation dynamics and imprint erasure through 5-hydroxymethylcytosine. Science, 339, 448-452. [CrossRef] [PubMed] [Google Scholar]
- Hajkova, P., Ancelin, K., Waldmann, T., Lacoste, N., Lange, U.C., Cesari, F., Lee, C., Almouzni, G., Schneider, R., Surani, M.A. (2008) Chromatin dynamics during epigenetic reprogramming in the mouse germ line. Nature, 452, 877-881. [CrossRef] [PubMed] [Google Scholar]
- Hammoud, S.S., Nix, D.A., Zhang, H., Purwar, J., Carrell, D.T., Cairns, B.R. (2009). Distinctive chromatin in human sperm packages genes for embryo development. Nature, 460, 473-478. [CrossRef] [PubMed] [Google Scholar]
- Hao, C., Gély-Pernot, A., Kervarrec, C., Boudjema, M., Becker, E., Khil, P., Tevosian, S., Jégou, B., Smagulova, F. (2016). Exposure to the widely used herbicide atrazine results in deregulation of global tissue-specific RNA transcription in the third generation and is associated with a global decrease of histone trimethylation in mice. Nucleic Acids Res, 44, 9784-9802. [PubMed] [Google Scholar]
- Joubert, B.R., Felix, J.F., Yousefi, P., Bakulski, K.M., Just, A.C., Breton, C., Reese, S.E., Markunas, C.A., Richmond, R.C., Xu, C.J., Küpers, L. K., Oh, S. S., Hoyo, C., Gruzieva, O., Söderhäll, C., Salas, L.A., Baïz, N., Zhang, H., Lepeule, J., Ruiz, C., Ligthart, S., Wang, T., Taylor, J.A., Duijts, L., Sharp, G.C., Jankipersadsing, S.A., Nilsen, R.M., Vaez, A., Fallin, M.D., Hu, D., Litonjua, A.A., Fuemmeler, B.F., Huen, K., Kere, J., Kull, I., Munthe-Kaas, M.C., Gehring, U., Bustamante, M., Saurel-Coubizolles, M.J., Quraishi, B.M., Ren, J., Tost, J., Gonzalez, J.R., Peters, M.J., Håberg, S.E., Xu, Z., Van Meurs, J.B., Gaunt, T.R., Kerkhof, M., Corpeleijn, E., Feinberg, A.P., Eng, C., Baccarelli, A.A., Benjamin Neelon, S.E., Bradman, A., Merid, S.K., Bergström, A., Herceg, Z., Hernandez-Vargas, H., Brunekreef, B., Pinart, M., Heude, B., Ewart, S., Yao, J., Lemonnier, N., Franco, O.H., Wu, M.C., Hofman, A., McArdle, W., Van der Vlies, P., Falahi, F., Gillman, M.W., Barcellos, L.F., Kumar, A., Wickman, M., Guerra, S., Charles, M.A., Holloway, J.,Auffray, C., Tiemeier, H.W., Smith, G.D., Postma, D., Hivert, M.F., Eskenazi, B., Vrijheid, M., Arshad, H., Antó, J.M., Dehghan, A., Karmaus, W., Annesi-Maesano, I., Sunyer, J., Ghantous, A., Pershagen, G., Holland, N., Murphy, S.K., DeMeo, D.L., Burchard, E.G., Ladd-Acosta, C., Snieder, H., Nystad, W., Koppelman, G.H., Relton, C.L., Jaddoe, V.W.V., Wilcox, A., Melén, E., London, S.J. (2016). DNA methylation in newborns and maternal smoking in pregnancy: Genome-wide consortium meta-analysis. Am J Human Genet, 98, 680-696. [CrossRef] [Google Scholar]
- Khashan, A.S., McNamee, R., Henriksen, T.B., Pedersen, M.G., Kenny, L.C., Abel, K.M., Mortensen, P.B. (2011). Risk of affective disorders following prenatal exposure to severe life events: A Danish population-based cohort study. J Psychiatr Res, 45, 879-885. [CrossRef] [PubMed] [Google Scholar]
- Klosin, A., Casas, E., Hidalgo-Carcedo, C., Vavouri, T., Lehner. B. (2017). Transgenerational transmission of environmental information in C.elegans. Science, 356, 320-323. [CrossRef] [PubMed] [Google Scholar]
- Lane, N., Dean, W., Erhardt, S., Hajkova, P., Surani, A., Walter, J., Reik, W. (2003). Resistance of IAPs to methylation reprogramming may provide a mechanism for epigenetic inheritance in the mouse. Genesis, 35, 88-93. [CrossRef] [PubMed] [Google Scholar]
- Laplante, D.P., Brunet, A., Schmitz, N., Ciampi, A., King, S. (2008). Project Ice Storm: Prenatal maternal stress affects cognitive and linguistic functioning in 5 1/2-year-old children. J Am Acad Child Adolesc Psychiatry, 47, 1063-1072. [CrossRef] [PubMed] [Google Scholar]
- Legoff, L., D’Cruz, S.C., Tevosian, S., Primig, M., Smagulova, F. (2019). Transgenerational inheritance of environmentally induced epigenetic alterations during mammalian development. Cells, 8, 1559. [CrossRef] [PubMed] [Google Scholar]
- Legoff, L., D’Cruz, S.C., Bouchekhchoukha, K., Monfort, C., Jaulin, C., Multigner, L., Smagulova, F. (2021). In utero exposure to chlordecone affects histone modifications and activates LINE-1 in cord blood. Life Science Alliance, 4, e202000944. [CrossRef] [PubMed] [Google Scholar]
- Li, J., Na, L., Ma, H., Zhang, Z., Li, T., Lin, L., Li, Q., Sun, C., Li, Y. (2015). Multigenerational effects of parental prenatal exposure to famine on adult offspring cognitive function. Sci Rep, 5, 13792. [CrossRef] [PubMed] [Google Scholar]
- Li, J., Liu, S., Li, S., Feng, R., Na, L., Chu, X., Wu, X., Niu, Y., Sun, Z., Han, T., Deng, H., Meng, X., Xu, H., Zhang, Z., Qu, Q., Zhang, Q., Li, Y., Sun, C. (2017). Prenatal exposure to famine and the development of hyperglycemia and Type 2 diabetes in adulthood across consecutive generations: A population-based cohort study of families in Suihua, China. Am J Clin Nutr, 105, 221-227. [CrossRef] [MathSciNet] [PubMed] [Google Scholar]
- Li, Q.D., Li, H., Li, F.J., Wang, M.S., Li, Z.J., Han, J., Li, Q.H., Ma, X.J., Wang, D.N. (2012). Nutrition deficiency increases the risk of stomach cancer mortality. BMC Cancer, 12, 315. [CrossRef] [PubMed] [Google Scholar]
- Lismer, A., Siklenka, K., Lafleur, C., Dumeaux, V., Kimmins, S. (2020). Sperm histone H3 Lysine 4 trimethylation is altered in a genetic mouse model of transgenerational epigenetic inheritance. Nucleic Acids Res, 48, 11380–11393. [CrossRef] [PubMed] [Google Scholar]
- Liu, J., Shi, J., Hernandez, R., Li, X., Konchadi, P., Miyake, Y., Chen, Q., Zhou, T., Zhou, C. (2023). Paternal phthalate exposure-elicited offspring metabolic disorders are associated with altered sperm small RNAs in mice. Environ Int, 172, 107769. [CrossRef] [PubMed] [Google Scholar]
- Lumey, L. H., Van Poppel, F.W. (1994). The Dutch famine of 1944-45: Mortality and morbidity in past and present generations. Soc Hist Med, 7, 229-246. [CrossRef] [PubMed] [Google Scholar]
- Molaro, A., Hodges, E., Fang, F., Song, Q., McCombie, W.R., Hannon, G.J., Smith, A.D. (2011). Sperm methylation profiles reveal features of epigenetic inheritance and evolution in primates. Cell, 146, 1029-1041. [CrossRef] [PubMed] [Google Scholar]
- Mustieles, V., Rodríguez-Carrillo, A., Vela-Soria, F., D’Cruz, S.C., David, A., Smagulova, F., Mundo-López, A., Olivas-Martínez, A., Reina-Pérez, I., Olea N., Freire, C., Arrebola, J.P., Fernández, M.F. (2022). BDNF as a potential mediator between childhood BPA exposure and behavioral function in adolescent boys from the INMA-Granada cohort. Sci Total Environ, 803, 150014. [CrossRef] [PubMed] [Google Scholar]
- Nixon, B., Stanger, S.J., Mihalas, B.P., Reilly, J.N., Anderson, A.L., Tyagi, S., Holt, J.E., McLaughlin, E.A. (2015). The microRNA signature of mouse spermatozoa is substantially modified during epididymal maturation. Biol Reprod, 93, 91. [CrossRef] [PubMed] [Google Scholar]
- Okano, M., Bell, D.W., Haber, D.A., Li., E. (1999). DNA methyltransferases Dnmt3a and Dnmt3b are essential for de novo methylation and mammalian development. Cell, 99, 247-257. [CrossRef] [PubMed] [Google Scholar]
- Oswald, J., Engemann, S., Lane, N., Mayer, W., Olek, A., Fundele, R., Dean, W., Reik, W., Walter, J. (2000). Active demethylation of the paternal genome in the mouse zygote. Curr Biol, 10, 475-478. [CrossRef] [PubMed] [Google Scholar]
- Pépin, A.S., Lafleur, C., Lambrot, R., Dumeaux, V., Kimmins, S. (2022). Sperm histone H3 Lysine 4 Tri-Methylation serves as a metabolic sensor of paternal obesity and is associated with the inheritance of metabolic dysfunction. Mol Metab, 59, 101463. [CrossRef] [PubMed] [Google Scholar]
- Rodney, N.C., Mulligan, C.J. (2014). A biocultural study of the effects of maternal stress on mother and newborn health in the Democratic Republic of Congo. Am J Phys Anthropol, 155, 200-209. [CrossRef] [PubMed] [Google Scholar]
- Rosenberg, T., Marco, A., Kisliouk, T., Haron, A., Shinder, D., Druyan, S., Meiri, N. (2022). Embryonic heat conditioning in chicks induces transgenerational heat/immunological resilience via methylation on regulatory elements. FASEB J, 36, e22406. [CrossRef] [PubMed] [Google Scholar]
- Russo, G., Landi, R., Pezone, A., Morano, A., Zuchegna, C., Romano, A., Muller, M.T., Gottesman, M.E., Porcellini, A., Avvedimento, E.V. (2016). DNA damage and repair modify DNA methylation and chromatin domain of the targeted locus: Mechanism of allele methylation polymorphism. Sci Rep, 6, 33222. [CrossRef] [PubMed] [Google Scholar]
- Sachs, M., Onodera, C., Blaschke, K., Ebata, K.T., Song, J.S., Ramalho-Santos, M. (2013). Bivalent chromatin marks developmental regulatory genes in the mouse embryonic germline in vivo. Cell Rep, 3, 1777-1784. [CrossRef] [PubMed] [Google Scholar]
- Seisenberger, S., Andrews, S., Krueger, F., Arand, J., Walter, J., Santos, F., Popp, C., Thienpont, B., Dean, W., Reik, W. (2012). The dynamics of genome-wide DNA methylation reprogramming in mouse primordial germ cells. Mol Cell, 48, 849-862. [CrossRef] [PubMed] [Google Scholar]
- Sharma, U., Sun, F., Conine, C.C., Reichholf, B., Kukreja, S., Herzog, V.A., Ameres, S.L., Rando, O.J. (2018). Small RNAs are trafficked from the epididymis to developing mammalian sperm. Dev Cell, 46, 481-494. [CrossRef] [PubMed] [Google Scholar]
- Shi, M., Whorton, A.E., Sekulovski, N., MacLean, J.A., Hayashi, K. (2019). Prenatal exposure to Bisphenol A, E, and S induces transgenerational effects on male reproductive functions in mice. Toxicol Sci, 172, 303–315. [CrossRef] [PubMed] [Google Scholar]
- Shi, Z., Zhang, C., Zhou, M., Zhen, S., Taylor, A.W. (2013). Exposure to the Chinese famine in early life and the risk of anaemia in adulthood. BMC Public Health, 13, 904. [CrossRef] [PubMed] [Google Scholar]
- Van Abeelen, A.F.M., de Rooij, S.R., Osmond, C., Painter, R. C., Veenendaal, M.V.E., Bossuyt, P.M.M., Elias, S.G., Grobbee, D. E., Van der Schouw, Y.T., Barker, D.J.P., Roseboom, T.J. (2011). The sex-specific effects of famine on the association between placental size and later hypertension. Placenta, 32, 694-698. [CrossRef] [PubMed] [Google Scholar]
- Veenendaal, M.V.E., Painter, R.C., de Rooij, S.R., Bossuyt, P.M.M., van der Post, F J.A.M., Gluckman, P.D., Hanson, M.A., Roseboom, T.J. (2013). Transgenerational effects of prenatal exposure to the 1944–45 Dutch famine. BJOG, 120, 548-553. [CrossRef] [PubMed] [Google Scholar]
- Wang, J., Li, Y., Han, X., Liu, B., Hu, H., Wang, F., Li, X., Yang, K., Yuan, J., Yao, P., Miao, X., Wei, S., Wang, Y., Liang, Y., Zhang, X., Guo, H., Yang, H., Hu, F.B., Wu, T., He, M. (2016). Exposure to the Chinese famine in childhood increases Type 2 diabetes risk in adults. J Nutr, 146, 2289-2295. [CrossRef] [PubMed] [Google Scholar]
- Zhang, B., Zheng, H., Huang, B., Li, W., Xiang, Y., Peng, X., Ming, J., Wu, X., Zhang, Y., Xu, Q., Liu, W., Kou, X., Zhao, Y., He, W., Li, C., Chen, B., Li, Y., Wang, Q., Ma, J., Yin, Q., Kee, K., Meng, A., Gao, S., Xu, F., Na, J., Xie, W. (2016). Allelic reprogramming of the histone modification H3K4me3 in early mammalian development. Nature, 537, 553-557. [CrossRef] [PubMed] [Google Scholar]
Citation de l’article : Smagulova, F. (2023). L’héritage épigénétique multigénérationnel chez l’Homme : le passé, le présent et les perspectives. Biologie Aujourd’hui, 217, 233-243
Liste des figures
 |
Figure 1 Changements de méthylation de l’ADN à la suite de la recombinaison homologue. Les cassures double-brin induisent la méthylation de l’ADN si les cassures se produisent pendant la phase de synthèse de l’ADN et si elles sont réparées via un mécanisme de recombinaison homologue. |
| Dans le texte | |
 |
Figure 2 Quelques preuves d’hérédité épigénétique transgénérationnelle dans des organismes modèles. |
| Dans le texte | |
 |
Figure 3 Analyse phénotypique et épigénétique dans les études transgénérationnelles. Pour l’analyse des effets induits par des facteurs exogènes, plusieurs paramètres sont pris en compte ; par exemple, l’analyse de coupes de tissus colorées à l’hématoxyline-éosine peut révéler des changements morphologiques. Des marqueurs spécifiques aideront à identifier plus finement d’éventuels changements dans les cellules. Enfin, en utilisant la technique des ‘omiques’, on peut analyser les changements à l’échelle génomique. Cette dernière approche a notamment permis de révéler de nouveaux biomarqueurs des effets de l’atrazine (Hao et al., 2016). L’analyse (par CHIP-seq) a montré une augmentation des marques H3K4me3 au niveau du promoteur du gène Pou5f1 dans les testicules mâles F1 et F3 suite à l’exposition prénatale à l’herbicide atrazine. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.


