Figure 8
Download original image
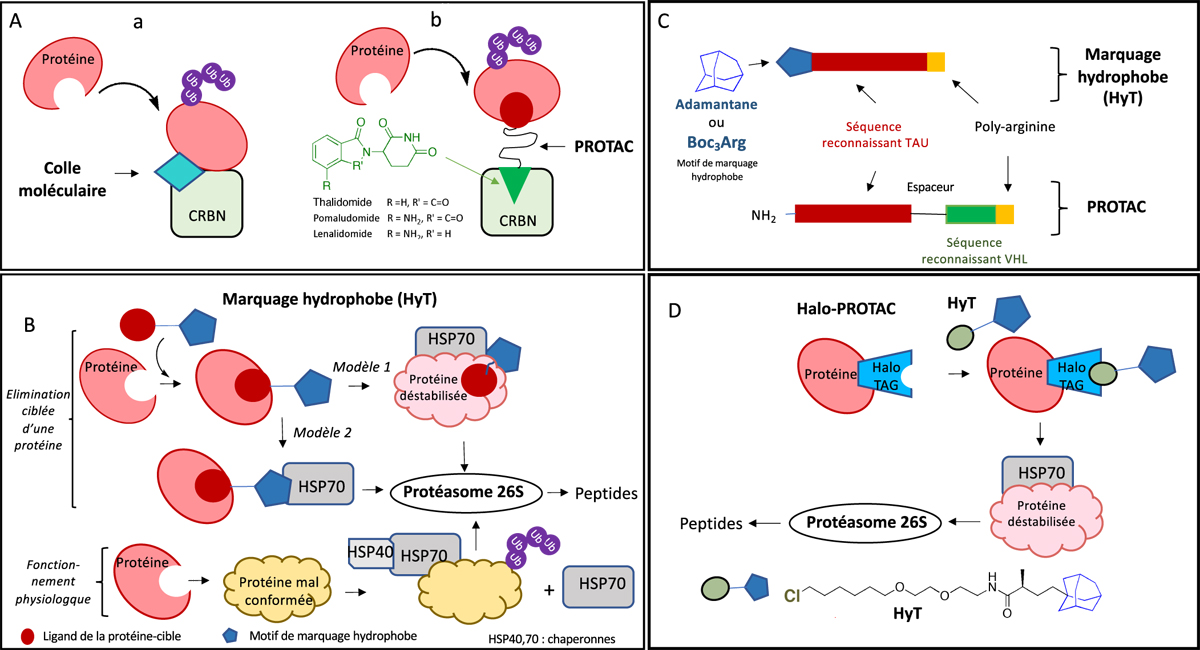
Comparaison entre les stratégies de dégradation induite par les PROTAC et par marquage hydrophobe (colle moléculaire) basé ou non sur HaloTag. A. Schématisation de l’interaction entre une protéine-cible et une E3 (CRBN) médiée par une colle moléculaire (a) ou un PROTAC (b). Le poids moléculaire de la colle moléculaire est inférieur à celui du PROTAC. B. Dégradation d’une protéine cible induite par une molécule HyT conduisant à un repliement incorrect. La molécule HyT provoque la déstabilisation de la conformation de la protéine avec complexation à HSP70 (modèle 1) ou une complexation directe avec HSP70 (modèle 2) conduisant dans les deux cas à une dégradation par le protéasome 26S. Le fonctionnement physiologique pour une protéine mal conformée est indiqué pour comparaison. C. Élaboration d’une molécule HyT ciblant la protéine Tau. Un motif hydrophobe adamantyle ou Boc3Arg est lié par covalence à un peptide reconnaissant spécifiquement Tau, le motif poly-arginine favorisant la pénétration cellulaire. La structure d’un PROTAC dégradant la protéine Tau est indiquée pour comparaison. D. Marquage hydrophobe sur une protéine de fusion HaloTag. La protéine de fusion « protéine d’intérêt-HaloTag » est reconnue par une molécule bifonctionnelle. L’état partiel de dénaturation qu’elle induit provoque la dégradation par le protéasome.
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.


