| Issue |
Biologie Aujourd’hui
Volume 217, Number 3-4, 2023
|
|
|---|---|---|
| Page(s) | 161 - 182 | |
| DOI | https://doi.org/10.1051/jbio/2023028 | |
| Published online | 29 novembre 2023 | |
Article
Intérêt et mécanismes d’action de la kétamine dans le traitement de l’addiction à l’alcool – Revue des études cliniques et précliniques
Interest and mechanisms of action of ketamine in alcohol addiction– A review of clinical and preclinical studies
Groupe de recherche sur l’alcool et les pharmacodépendances, INSERM U1247, CURS, Amiens, France
* Auteurs correspondants : Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
; Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Reçu :
19
Mai
2023
Résumé
Le Trouble de l’Usage d’Alcool (TUA) est une maladie psychiatrique caractérisée par une consommation chronique et excessive d’alcool malgré des conséquences négatives sur la santé et le fonctionnement social ou professionnel. Les options de traitements du TUA sont actuellement limitées et les tailles d’effet et taux de réponse à ces traitements sont souvent faibles à modérés. L’Organisation Mondiale de la Santé a identifié le développement des médicaments pour traiter le TUA comme l’une de ses 24 priorités. Cette dernière décennie a été marquée par un intérêt renouvelé pour l’utilisation de psychédéliques en psychiatrie. La kétamine, un psychédélique atypique déjà utilisé dans le traitement de la dépression majeure, est au centre de cette renaissance. Cet antagoniste des récepteurs NMDA existe sous deux formes énantiomères, la S-kétamine et la R-kétamine, qui peuvent être métabolisées en différents dérivés, dont certains ont montré des propriétés antidépressives. Cet article de revue vise à faire le bilan des études cliniques et précliniques sur l’utilisation de la kétamine et de ses métabolites dans le traitement du TUA. L’ensemble de ces études montre que la kétamine est efficace pour réduire les symptômes de sevrage et les envies irrépressibles d’alcool. Les propriétés antidépressives avérées de la kétamine contribuent à la diminution du risque de rechute dans le mésusage d’alcool, notamment chez les patients suivant des psychothérapies. Son efficacité est supposée être liée à sa capacité à réguler la voie glutamatergique, à améliorer la neuroplasticité, à réorganiser la connectivité fonctionnelle des réseaux d’état de repos (resting state networks) du cerveau et à réduire les états dépressifs. Bien que ces premiers résultats soient prometteurs, la mise en évidence de différences importantes entre les sexes, et la méconnaissance du rôle de chacun des métabolites dans les effets observés justifient la poursuite des recherches précliniques pour mieux comprendre comment agissent véritablement la kétamine et ses métabolites sur le TUA. En clinique, les études récentes s’intéressent désormais à la dépendance à la kétamine et à la dépression comorbide, ainsi qu’à l’influence du sexe, une comorbidité plus forte entre la dépendance à l’alcool et la dépression semblant exister chez la femme.
Abstract
Alcohol Use Disorder (AUD) is a psychiatric condition characterized by chronic and excessive drinking despite negative consequences on overall health and social or occupational functioning. There are currently limited treatment options available for AUD, and the effects size and the response rates to these treatments are often low to moderate. The World Health Organization has identified the development of medications to treat AUD as one of its 24 priorities. This past decade was marked by a renewed interest in psychedelic use in psychiatry. At the centre of this renaissance, ketamine, an atypical psychedelic already used in the treatment of major depression, is an NMDA receptor antagonist that exists as a racemic compound made of two enantiomers, S-ketamine, and R-ketamine. Each form can be metabolized into different metabolites, some of which having antidepressant properties. In this article, we review both clinical and preclinical studies on ketamine and its metabolites in the treatment of AUD. Preclinical as well as clinical studies have revealed that ketamine is effective in reducing withdrawal symptoms and alcohol craving. Convergent data showed that antidepressant properties of ketamine largely contribute to the decreased likelihood of alcohol relapse, especially in patients undergoing ketamine-assisted psychotherapies. Its effectiveness is believed to be linked with its ability to regulate the glutamatergic pathway, enhance neuroplasticity, rewire brain resting state network functional connectivity and decrease depressive-like states. However, it remains to further investigate (i) why strong differences exist between male and female responses in preclinical studies and (ii) the respective roles of each of the metabolites in the ketamine effects in both genders. Interestingly, current studies are also focusing on ketamine addiction and the comorbidity between alcohol addiction and depression occurring more frequently in females.
Mots clés : kétamine / alcool / psychédéliques / trouble de l’usage d’alcool / neurobiologie
Key words: ketamine / alcohol / psychedelics / alcohol use disorder / neurobiology
© Société de Biologie, 2023
Abréviations
2R,6R-HK : 2R,6R-hydroxykétamine
2S,6S-HK : 2S,6S-hydroxykétamine
AIC : Cortex insulaire agranulaire
BDNF : Brain Derived Neurotrophic Factor
BLA : Amygdale basolatérale
BZD : Benzodiazépines
CBD : Cannabidiol
CIE : Inhalation chronique de vapeurs d’alcool
DID : Drinking In the Dark
DHNK : Dihydroxynorkétamine
HNK : Hydroxynorkétamine
IA2BC : Accès intermittent en situation de choix alcool/eau
MET : Motivational Enhancement Therapy
MRI : Mémoires des récompenses inadaptées
mTOR : Mammalian Target of Rapamycin
NBQX : 2,3-dioxo-6-nitro-7-sulfamoyl-benzo[f]quinoxaline
NMDA : N-méthyl-D-aspartate
PCP : Phéncyclidine
PTSD : Post Traumatic Stress Disorder (Syndrome de stress post-traumatique)
R-AMPA : Récepteur AMPA du glutamate
RM : Rappel mémoriel
RMD : Réseau de mode par défaut
R-NK : R-norkétamine
R-NMDA : Récepteur NMDA du glutamate
S-NK : S-norkétamine
TCC : Thérapie comportentale et cognitive
THC : Tétra-hydro-cannabinol
TPK : Thérapie psychédélique par kétamine
TRKB : Récepteur-tyrosine kinase à haute affinité pour le BDNF
TUA : Trouble de l’Usage d’Alcool
Introduction – La kétamine, un psychédélique atypique
Pendant la dernière décennie, la renaissance des psychédéliques a fait évoluer le regard de la communauté scientifique sur le potentiel thérapeutique d’un grand nombre de molécules qui sont aussi des drogues. Parmi celles-ci, la MDMA (3,4-méthylènedioxy-méthamphétamine) et le THC (tétra-hydro-cannabinol) offrent des opportunités uniques pour le traitement de diverses pathologies, telles que le syndrome de stress post-traumatique (PTSD), l’anxiété, la dépression, la maladie d’Alzheimer, la maladie de Parkinson et les douleurs chroniques (Feduccia & Mithoefer, 2018 ; Bird et al., 2021 ; De Gregorio et al., 2021 ; Costa et al., 2022 ; Mendes et al., 2022 ; Modaresi & Talachian, 2022 ; Hameed et al., 2023 ; Hasbi et al., 2023 ; Li et al., 2023). D’autres alternatives non addictogènes, comme le CBD, présentent un effet thérapeutique encore débattu et considéré comme limité (Orsolini et al., 2019 ; Mendes et al., 2022). La kétamine, qui est un antagoniste non compétitif des récepteurs NMDA, a d’abord été utilisée en tant qu’anesthésique, mais très rapidement ses propriétés uniques au niveau du système glutamatergique ont suscité de l’intérêt pour le traitement de divers troubles mentaux. Le plus souvent étudiée sous la forme racémique, la kétamine, mais aussi ses deux énantiomères et leurs différents métabolites, présentent un large spectre d’actions au niveau de différents systèmes de neurotransmission. En 2019, un spray à base de S-kétamine a été approuvé et mis sur le marché en tant que traitement de dernier recours pour la dépression majeure résistante. La dépression et le Trouble de l’Usage d’Alcool (TUA) étant des pathologies duelles (co-occurrentes ou encore appelées « comorbidités ») (Grant & Harford, 1995), partageant des bases neurobiologiques communes, plusieurs études récentes suggèrent une efficacité de la kétamine dans le TUA (Ezquerra-Romano et al., 2018 ; De Gregorio et al., 2021 ; Walsh et al., 2021 ; Garel et al., 2022).
Histoire de la kétamine
La synthèse de dérivés de la phéncyclidine (PCP) a permis d’identifier dans les années 1960 un nouvel anesthésique d’abord appelé CI-581 et popularisé depuis sous le nom « kétamine » (Kolp et al., 2007 ; Kohtala, 2021). Ce composé se distinguait de la PCP par son mécanisme d’action rapide ainsi que la qualité de ses propriétés anesthésiques. En 1970, aux USA, la Food and Drug Administration approuve l’utilisation de la kétamine, qui se développe en particulier lors de la guerre du Viêtnam en tant qu’anesthésique, mais aussi en tant qu’analgésique (Kohtala, 2021). La kétamine se démarque par sa capacité à soulager rapidement des douleurs aiguës intenses, et à traiter des douleurs chroniques (Orhurhu et al., 2019), et cela avec un risque d’effets secondaires relativement faible. Dans les années 1990, de nouvelles études se sont intéressées aux effets de la kétamine chez des patients souffrant de schizophrénie, de dépression et du PTSD (De Gregorio et al., 2021). En plus de son intérêt thérapeutique, la kétamine devient rapidement une « drogue de soirée », et prend plusieurs noms, comme « Special-K » ou « Kit-Kat ». L’utilisation récréative et illégale de la kétamine entraîne sa classification en tant que « substance d’abus » de classe III, selon la loi sur les substances contrôlées aux États-Unis (Worrell & Gould, 2021). Toutefois, en 2000, une première étude randomisée contrôlée en double aveugle montre un effet antidépresseur d’une dose unique de kétamine (0,5 mg/kg) chez des patients souffrant de dépression majeure (Berman et al., 2000). Cette étude a par la suite été répliquée et validée par de nombreuses équipes (DiazGranados et al., 2010 ; Sos et al., 2013 ; Abdallah et al., 2018). De même, la S-kétamine a obtenu une autorisation de mise sur le marché et est indiquée en spray nasal sous l’appellation « Spravato Esketamine » pour le traitement de la dépression majeure résistante aux traitements (Sanders & Brula, 2021).
En plus de la dépression, le trouble de l’usage de drogues et notamment le TUA ont fait l’objet d’investigations cliniques en vue d’évaluer un éventuel bénéfice thérapeutique avec la kétamine dans ces pathologies (Condi et al., 1972 ; Krupitsky et al., 1992 ; Krupitsky & Grinenko, 1997). C’est ainsi que 16 études cliniques ont vu le jour, dont 5 sont en cours, évaluant l’efficacité et la sécurité de l’utilisation de la kétamine pour réduire la consommation d’alcool, maintenir l’abstinence et traiter le syndrome de sevrage alcoolique. Dans le présent article de revue, nous faisons le bilan des nombreuses études aussi bien cliniques que précliniques pertinentes qui permettent aujourd’hui de décrire les mécanismes probables à l’origine des effets thérapeutiques de la kétamine chez les patients présentant un TUA.
Neuropharmacologie de la kétamine
La kétamine est un hallucinogène dissociatif, qui fait partie de la famille des arylcyclohexylamines. C’est un mélange racémique de deux énantiomères en proportions égales, la S-Kétamine et la R-Kétamine (Jelen et al., 2021). L’atome de carbone qui porte la fonction méthyl-amine et le groupe chlorophényl est responsable de l’asymétrie qui conduit aux deux énantiomères de configuration absolue R et S, comme représentés sur la Figure 1. Le mécanisme d’action principal de la kétamine est l’antagonisme non compétitif des R-NMDA, qui à forte dose provoque une amnésie, une analgésie, une perception dissociée de l’environnement et une immobilité (Dakwar et al., 2014). En plus de ses effets sur le système glutamatergique, la kétamine modifie le fonctionnement d’un grand nombre d’autres neurotransmetteurs. Par exemple, elle bloque les canaux ioniques nicotiniques acétylcholinergiques (Lydic & Baghdoyan, 2002), et exerce des « effets renforçants » via son action sur les systèmes dopaminergique (Kokkinou et al., 2018) et opioïdergique (Williams et al., 2018). Des études récentes suggèrent que les effets « renforçants » sont principalement dus à la S-kétamine, l’énantiomère dit « actif » (Heifets et al., 2021 ; Shim, 2022). Les énantiomères et les différents métabolites de la kétamine modifient également d’autres voies cellulaires et moléculaires (Ezquerra-Romano et al., 2018 ; Jelen et al., 2021).
En clinique, le mélange racémique de kétamine est habituellement injecté par voie intra-veineuse, et parfois intra-musculaire, favorisant une distribution rapide dans l’ensemble de l’organisme (Ezquerra-Romano et al., 2018). De plus, la kétamine présente une solubilité lipidique élevée permettant une capacité d’action rapide. Initialement, elle est distribuée dans les tissus très perfusés, comme le cerveau, où elle produit ses premiers effets dans les 5 min après son administration. Sa clairance hépatique est élevée (1 L/min), son volume de distribution est grand (3 L/kg), et sa demi-vie d’élimination est de 2 h. Des doses de la forme racémique allant de 1 à 4,5 mg/kg sont utilisées pour induire et maintenir l’anesthésie (Peltoniemi et al., 2016), alors qu’en clinique des doses sous-anesthétiques sont utilisées pour induire des expériences de type psychédélique (Ezquerra-Romano et al., 2018 ; Walsh et al., 2021 ; Mendes et al., 2022). Parmi les effets psychotropes de la kétamine on observe des délires, des hallucinations, de la confusion et, à des doses plus élevées, des expériences extra-corporelles, de « mort imminente » ainsi que des expériences mystiques. Ces effets subjectifs, longtemps considérés comme négatifs, ont caractérisé la kétamine comme une drogue « psychotomimétique ». En outre, depuis de nombreuses années, la kétamine est utilisée en tant que modèle pharmacologique de la schizophrénie (Frohlich & Van Horn, 2014). L’ensemble de ces effets « secondaires » a inévitablement freiné son utilisation en clinique (Morgan et al., 2012 ; Olson, 2021). Cependant, récemment, certaines études semblent appuyer la nécessité des effets subjectifs de la kétamine dans son efficacité thérapeutique et soulignent l’utilité probable des effets psychédéliques dans le traitement des troubles mentaux (Dakwar et al., 2014 ; Grabski et al., 2020 ; Rothberg et al., 2021 ; Yaden & Griffiths, 2021 ; Dworkin et al., 2022 ; Mendes et al., 2022). Mais un autre axe de recherche soutient l’hypothèse opposée et donc plutôt le développement de psychédéliques non hallucinogènes pour des objectifs thérapeutiques (Cameron et al., 2021 ; Cao et al., 2022 ; Scotton et al., 2022).
La kétamine bloque les R-NMDA qui sont une composante majeure de la transmission glutamatergique, activés à la fois par la fixation du glutamate et une dépolarisation membranaire supraliminaire concomitante induite par l’activation des récepteurs AMPA (R-AMPA). La levée de l’inhibition des R-NMDA par le magnésium après activation des R-AMPA intervient dans le phénomène de potentialisation à long terme, un mécanisme cellulaire à la base de l’apprentissage et la mémorisation. Il existe aussi des R-NMDA au niveau présynaptique, ces derniers modulant la libération spontanée et évoquée de différents neurotransmetteurs. Le mécanisme d’action synaptique de la kétamine passerait par deux voies distinctes : la voie directe au travers de laquelle la kétamine bloque les R-NMDA du versant post-synaptique et donc empêche la dépolarisation du neurone postsynaptique, et la voie indirecte impliquant le blocage des R-NMDA des interneurones inhibiteurs gabaergiques, levant ainsi l’inhibition tonique de ces interneurones et augmentant de ce fait la libération de glutamate.
Ces deux mécanismes d’action impliquent les cascades intracellulaires calcium-dépendantes des cibles de la rapamycine chez les mammifères (mTORC1 et mTORC2), ainsi qu’une augmentation de la libération de facteurs neurotrophiques comme le BDNF (Brain Derived Neurotrophic Factor). L’activation différentielle de ces deux voies semble dépendre de la dose de kétamine, de la composition en sous-unités des R-NMDA, ainsi que de l’énantiomère de kétamine utilisé.
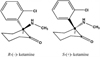 |
Figure 1 Les deux énantiomères de la kétamine. Ces deux énantiomères se différencient par leur conformation spatiale caractérisée par le carbone asymétrique noté 2 et conférant des propriétés physico-chimiques uniques à chaque énantiomère. Le groupement méthylamine NH-CH3 est dans le plan avant pour la R-kétamine et dans le plan arrière pour la S-kétamine. |
Les énantiomères et métabolites de la kétamine
Bien que la S-kétamine soit considérée comme le métabolite actif, puisqu’elle présente une affinité plus grande pour les R-NMDA que la R-kétamine (Ki = 0,30 µM et Ki = 1,4 µM, respectivement) (Jelen et al., 2021), des études récentes suggèrent que la R-kétamine présente également des propriétés thérapeutiques, notamment dans le traitement de la dépression (Zanos et al., 2016 ; Wei et al., 2020 ; Jelen et al., 2021 ; Scotton et al., 2022). Ces deux énantiomères sont métabolisés par les cytochromes P450 (Figure 2 ) (Jelen et al., 2021). La S-kétamine et la R-kétamine sont soit déméthylées pour donner respectivement la S-norkétamine (S-NK) et la R-norkétamine (R-NK), soit hydroxylées pour donner la 2S,6S-hydroxykétamine (2S,6S-HK) et la 2R,6R-hydroxykétamine (2R,6R-HK). Les formes hydroxylées 2S,6S-HK et 2R,6R-HK sont par la suite transformées en 2S,6S-hydroxynorkétamine (2S,6S-HNK) et 2R,6R-hydroxynorkétamine (2R,6R-HNK), les deux métabolites retrouvés dans le plasma à la suite de l’administration de kétamine (Zarate et al., 2012 ; Jelen et al., 2021). Les formes déméthylées S-NK et R-NK sont elles aussi métabolisées en 2S,6S-HNK et 2R,6R-HNK et, à un degré moindre, en S-dihydroxynorkétamine (S-DHNK) et R-dihydroxynorkétamine (R-DHNK) (Zarate et al., 2012 ; Jelen et al., 2021). Un intérêt particulier appelant l’étude des différents métabolites de la kétamine concerne les différences selon le sexe. L’une des principales enzymes impliquées dans la métabolisation de la kétamine est le cytochrome P450 3A4 (CYP3A4), dont les taux diffèrent chez l’homme et chez la femme. Des études suggèrent en effet que les femmes ont généralement des niveaux plus faibles de CYP3A4 que les hommes (Klein & Zanger, 2013). Par ailleurs, les concentrations plasmatiques de certains métabolites de la kétamine, en particulier la DHNK et la HNK, sont plus élevées chez les femmes que chez les hommes (Highland et al., 2022). Ces données sont aussi retrouvées chez le rat. Chez cette espèce, une étude montrant que les femelles sont plus sensibles aux effets antidépresseurs de la kétamine que les mâles a mis en avant, par des analyses plasmatiques et des prélèvements cérébraux, que les niveaux de kétamine et de norkétamine sont plus élevés chez les femelles (Saland & Kabbaj, 2018). La vitesse de métabolisation de la kétamine semble donc jouer un rôle important dans la puissance de son effet antidépresseur. De plus, comme les métabolites peuvent avoir des effets spécifiques, distincts de ceux de la kétamine racémique, notamment en ce qui concerne leurs effets antidépresseurs et analgésiques (Hess et al., 2022), des différences dans les concentrations plasmatiques de ces métabolites pourraient également contribuer aux différences de réponse à la kétamine entre les sexes.
Parmi ces autres métabolites, la norkétamine présente des propriétés antidépressives et anxiolytiques qui contribuent très probablement aux effets antidépresseurs du mélange racémique. À l’instar de la S-kétamine comparée à la R-kétamine, la S-norkétamine, présente une affinité plus grande pour les R-NMDA que la R-norkétamine. Une étude préclinique a par ailleurs montré le rôle de la S-norkétamine dans l’antagonisme des R-NMDA, notamment lorsque la kétamine est administrée par voie orale (Ebert et al., 1999). Cela souligne l’importance de la voie d’administration de la kétamine, ainsi que le besoin d’études spécifiques des effets antidépresseurs de la S-norkétamine. Récemment, d’autres études ont suggéré l’implication de l’hydroxynorkétamine (HNK) dans l’effet antidépresseur de la kétamine. Ce métabolite semble exercer des effets antidépresseurs indépendamment des R-NMDA (Zanos et al., 2016 ; Hess et al., 2022). Dans le cadre de la dépression, une augmentation de l’activation des récepteurs AMPA au niveau du cortex préfrontal et de l’hippocampe est identifiée chez les patients en rémission et semble jouer un rôle déterminant dans la réponse au traitement (Autry et al., 2011 ; Zanos et al., 2016). Or, la HNK, et plus précisément la (2R-6R)-HNK, active directement les R-AMPA (Yao et al., 2018), ainsi que les récepteurs mGluR2 du glutamate (Zanos et al., 2019), ce dernier effet contribuant aussi très probablement aux effets antidépresseurs de la kétamine (Moreno et al., 2011). Comme il a été démontré que l’alcoolodépendance entraîne une diminution de l’expression de ces récepteurs mGluR2, que ce soit dans des structures limbiques (Joffe et al., 2018), ou encore corticales (Meinhardt et al., 2013, 2021), la (2R-6R)-HNK pourrait également présenter un intérêt en tant que possible médicament du TUA (Strong & Kabbaj, 2020).
Bien que les interactions diverses entre les métabolites de la kétamine et le système glutamatergique soient une piste de recherche intéressante dans le cadre du TUA, la recherche actuelle concerne surtout l’évaluation de l’efficacité thérapeutique de la kétamine racémique sur ce trouble. Plus généralement, à l’avenir, il serait intéressant de déterminer le potentiel thérapeutique de la (2R-6R)-HNK et de la S-norkétamine au regard des différentes pathologies psychiatriques associées à des perturbations glutamatergiques.
 |
Figure 2 La kétamine et les principaux métabolites de ses énantiomères. La S-kétamine et la R-kétamine sont d’abord métabolisées respectivement en S-norkétamine ou en R-norkétamine par les cytochromes P450. Ces deux premiers métabolites peuvent être métabolisés de nouveau pour donner la S-déhydronorkétamine (S-DHNK) ou la R-déhydronorkétamine (R-DHNK). Parallèlement la S-kétamine et la R-kétamine peuvent aussi être hydroxylées en S-hydroxykétamine (2S-6S-HK) et R-hydroxykétamine (2R-6R-HK) via le cytochrome PA6 puis ensuite métabolisées en 2S-6S-hydroxynorkétamine (2S-6S-HNK) et en 2R-6R-hydroxynorkétamine (2R-6R-HNK). |
Traitement de l’alcoolodépendance avec la kétamine – Études cliniques et précliniques
Pour faire le point sur cette question, nous avons analysé les données de 6 revues publiées récemment, chacune consacrée principalement, ou en partie, à la kétamine dans le traitement du trouble de l’usage de drogues dont l’alcool (Ezquerra-Romano et al., 2018 ; Walsh et al., 2021 ; Worrell & Gould, 2021 ; Garel et al., 2022 ; Mendes et al., 2022 ; Goldfine et al., 2023). Ces revues ont ensuite été utilisées pour sélectionner l’ensemble des études cliniques, et – lorsque cela était possible – des études précliniques, en rapport avec la problématique de l’addiction à l’alcool. Des recherches complémentaires ont par la suite été réalisées afin de s’assurer qu’aucun autre article clinique ou préclinique n’était disponible. Au total, après sélection par le doctorant premier auteur (H.F.F), et vérification par les deux autres co-auteurs plus expérimentés (M.N, J.J), 11 études cliniques et 11 études précliniques ont été retenues pour notre analyse. De plus, les résumés de 5 études cliniques en cours ont pu être obtenus. Dans l’ensemble, les études cliniques les plus anciennes datent de 1992, et les plus récentes de 2022, et les études pré-cliniques les plus anciennes datent de 2002 et les plus récentes de 2022.
Études cliniques
Le Tableau 1 montre l’ensemble des études cliniques qui, à date, ont évalué l’efficacité de la kétamine dans le traitement du TUA (N = 8) ou du syndrome de sevrage alcoolique (N = 3).
Les premières études utilisant la kétamine dans le traitement de l’addiction se sont déroulées entre 1964 et 1974 au Mexique. Différents psychédéliques ont été administrés, notamment du LSD et de la kétamine, à des personnes volontaires, mais dans un cadre non contrôlé. Ces expériences ont conduit en 1975 à l’incarcération de Salvador Roquet qui les avait encadrées. Quelques années plus tard, deux études cliniques en Russie ont été publiées (Krupitsky et al., 1992 ; Krupitsky & Grinenko, 1997), rapportant l’utilisation d’une thérapie psychédélique par kétamine (TPK) pour réduire la rechute de patients atteints de TUA et récemment sevrés (Ezquerra-Romano et al., 2018). Les deux études portaient sur un ensemble de résultats issus d’études cliniques contrôlées mais non randomisées, réalisées sur une à plusieurs années. Dans les deux cas, les auteurs ont privilégié une approche thérapeutique dite « aversive », basée sur une prise de conscience des effets néfastes de l’alcool sur la vie quotidienne du participant. Cette intervention thérapeutique au sein de la « TPK » est nommée « The Affective Contra Attribution Method ».
Dans la première étude, les patients sont répartis en deux groupes, le premier groupe de 86 participants recevra la kétamine (3 mg/kg, en intramusculaire) et le second groupe, de 100 participants, uniquement la thérapie aversive. Avant l’intervention, tous les patients s’entretiennent avec le psychothérapeute. Le patient est d’abord informé que la kétamine induira un état de conscience altérée dans lequel il se rendra compte des effets négatifs de l’alcool sur sa vie, et verra les côtés positifs de la sobriété, et que cela permettra d’éliminer les attitudes inconscientes envers l’alcool. Cette prise de conscience se fera en association via des hallucinations émotives, construites pour introduire les aspects négatifs du TUA dans la conscience, et ainsi fournir une base pour une sobriété continue (Krupitsky et al., 1992). Avant l’intervention pharmacologique et en complément de la kétamine, les patients reçoivent du bémégride, qui potentialise les effets psychotropes de la kétamine, ainsi que de l’aethimizol, qui favorise la mise en mémoire de l’expérience. Afin d’induire l’apparition des hallucinations aversives ciblées, les auteurs expliquent qu’au pic des effets hallucinogènes, l’odeur et le goût de l’alcool sont introduits pendant que le thérapeute communique avec le patient sur un fond musical dramatique. Après la session de kétamine, les deux groupes reçoivent une psychothérapie de groupe pour faciliter l’intégration et la compréhension de l’expérience psychédélique. La publication rapporte que parmi les participants ayant reçu de la kétamine, 69,9 % sont restés abstinents 1 an après l’intervention versus 24 % pour le groupe ne bénéficiant que de la thérapie par aversion (Krupitsky et al., 1992). Cette procédure a été utilisée chez plus de 1000 personnes alcoolodépendantes sans complications ou effets secondaires graves signalés (Krupitsky et al., 1992 ; Krupitsky & Grinenko, 1997).
Dans la deuxième étude, Krupitsky & Grinenko (1997) notent les taux de rechutes de patients ayant suivi un programme de désintoxication d’une durée de 3 mois. Ces derniers avaient le choix entre recevoir la thérapie TPK, incluant la kétamine (2,5 mg/kg, en intramusculaire N = 111), ou un traitement médicamenteux usuel couplé à de la psychothérapie conventionnelle (N = 100). Les auteurs rapportent qu’un an après l’intervention, 65,8 % des patients (73/111) ayant reçu la kétamine sont encore abstinents, contre 24 % (24/100) pour le groupe témoin. De plus, deux et trois ans après le traitement, le taux d’abstinence des patients du groupe kétamine est de 40,7 % (33 sur 81 patients) et de 33,3 % (14 sur 42 patients) respectivement. À noter cependant que 88 patients ont été exclus de l’étude longitudinale, notamment par souci de correspondance. Enfin, les patients rapportent une relation avec l’alcool plus saine, et un changement positif dans divers aspects de leur vie.
Bien que ces premières études indiquent une efficacité et une sécurité de l’utilisation de la kétamine dans le TUA, elles présentent certaines limites. Principalement, le groupe témoin ne reçoit aucun placebo, et le contenu de leur psychothérapie diffère grandement de la thérapie TPK. De plus, aucune randomisation n’a été faite puisque les patients du groupe actif ont choisi volontairement de recevoir la kétamine. Un biais quant à la motivation du patient pour l’arrêt de la consommation est donc possible. Ainsi ces deux limites pourraient avoir contribué aux différences d’abstinence observées. Toutefois, les auteurs soulignent dans leur discussion que ces taux d’abstinence restent significativement supérieurs à ceux retrouvés avec un traitement standard (Garel et al., 2022).
Des années auparavant, en 1972, une équipe française, Condi et al. (1972), s’est intéressée à l’utilisation de la kétamine dans le cadre de la réduction des symptômes de sevrage. Huit hommes et une femme, admis en soins intensifs et présentant un delirium tremens, ont reçu de la kétamine tout au long de leur hospitalisation. La durée de traitement était variable, comprise entre 1 et 7 jours, et les doses de kétamine utilisées étaient comprises entre 5 et 20 mg/kg en intramusculaire ou entre 4 et 6 mg/kg en intraveineux. Peu d’informations sont disponibles quant aux spécificités de cette étude, toutefois les patients ont également reçu des tranquillisants (pentobarbital et méprobamate). Les auteurs décrivent une réduction de l’agitation des patients 2 à 3 minutes après l’administration de kétamine (Condi et al., 1972 ; Garel et al., 2022). Bien que les limites soient évidentes, cette étude suggère que la kétamine pourrait induire une réduction des symptômes de sevrage.
Trente ans plus tard, entre 2015 et fin 2018, trois études cliniques ont poursuivi l’évaluation de l’efficacité de la kétamine dans la réduction des symptômes de sevrage, et se sont intéressées à l’administration adjuvante de kétamine avec des benzodiazépines (BZD) dans le cas du sevrage alcoolique sévère (Wong et al., 2015 ; Pizon et al., 2018 ; Shah et al., 2018). Ces trois études sont similaires en termes d’intervention chez des patients admis en unité de soins intensifs, et présentant un syndrome de sevrage alcoolique. La kétamine est administrée par voie intraveineuse, en complément des agents pharmacologiques classiques (lorazépam ou une autre BZD), sans psychothérapie préventive ou de suivi, à des doses sous-anesthésiques variant entre 0,15 et 0,75 mg/kg/h. Les patients sont ensuite évalués à l’aide de l’échelle CIWA (Clinical Institute Withdrawal Assessment), un outil servant à l’évaluation de l’intensité des symptômes de sevrage (Condi et al., 1972 ; Wong et al., 2015 ; Pizon et al., 2018 ; Shah et al., 2018 ; Dakwar et al., 2020). En outre, ont été également notés le comportement durant l’intervention (Condi et al., 1972), l’évolution du risque d’intubation (Pizon et al., 2018) et l’évolution du besoin en BZD pour réduire les symptômes de sevrage (Wong et al., 2015 ; Pizon et al., 2018 ; Shah et al., 2018).
La première étude est celle de Wong et al. (2015), dans laquelle 23 patients ont été admis en soins intensifs pour sevrage alcoolique. Le diagnostic de delirium tremens étant établi, ces patients ont été traités avec des BZD, mais n’y ont pas répondu. Le traitement à la kétamine a démarré 33,6 h après l’admission, à la dose moyenne de 0,21 mg/kg/h. Douze heures après l’initiation de ce traitement à la kétamine, le besoin en BZD avait diminué de 40 mg, et 24 h après de 13,3 mg. Ces résultats sont significatifs (p = 0,110 et p = 0,330, respectivement). En moyenne, les patients sont restés 5,6 jours en soins intensifs avant la résolution des symptômes de sevrage. Cette première étude confirme les observations de Condi et al. (1972) et semble indiquer que la kétamine est relativement sans danger lorsqu’elle est administrée dans cette configuration, puisque seul un patient a présenté un effet secondaire lié à un surdosage. Toutefois, dans cette étude, la kétamine n’était pas le seul composé utilisé en complément des BZD. D’autres traitements symptomatiques ont été administrés en complément (Wong et al., 2015). Cela, ainsi que l’absence d’un groupe témoin, limitent la portée de cette étude (Goldfine et al., 2023).
La seconde étude est celle de Pizon et al. (2018), dont la cohorte est constituée de 63 patients ayant été admis en soins intensifs pour sevrage alcoolique. Dans cette étude, la moitié des patients reçoit des traitements symptomatiques (agonistes gabaergiques se substituant à l’éthanol) ou du lorazépam (N = 29) et le groupe actif reçoit les mêmes traitements mais avec la kétamine en complément (N = 34). La kétamine, comme l’ensemble des autres traitements, est administrée en intraveineux à une dose moyenne de 0,15 mg/kg/h pendant 47 h. Dans certains cas, lorsque le delirium tremens était jugé très sévère, la kétamine était augmentée à 0,3 mg/kg/h. En moyenne, l’ensemble des symptômes a disparu dans la première heure de traitement avec la kétamine. Une diminution significative de plus de 2 jours de la durée moyenne d’hospitalisation a été relevée uniquement pour le groupe ayant reçu la kétamine. Les résultats principaux indiquent que la kétamine diminue le besoin en BZD (dont le lorazépam), sans induire de risque particulier dans le cadre du sevrage alcoolique (Pizon et al., 2018).
La troisième étude est celle de Shah et al. (2018), qui inclut des patients admis en soins intensifs pour sevrage alcoolique. Le traitement initial consistait en une perfusion continue de lorazépam (8 mg en intraveineux toutes les 15 minutes, 3 doses maximum) et de phénobarbital (260 mg, puis 130 mg en intraveineux toutes les 15 minutes, 8 doses maximum). Si les symptômes perduraient, alors une perfusion de lorazépam (14 mg/h) était ajoutée. Sur l’ensemble des admissions en soins intensifs, 30 patients présentaient un sevrage alcoolique résistant au lorazépam, et ont donc été isolés afin de recevoir une perfusion supplémentaire de kétamine. Celle-ci a été administrée par voie intraveineuse à des doses comprises entre 0,5 et 4,5 mg/kg/h. Pour l’ensemble des patients, une diminution des symptômes 1 h après le début de perfusion a été observée, et 24 h après, le besoin en BZD a été réduit de 28 % (Shah et al., 2018). Cependant, l’intervention thérapeutique n’ayant pas été contrôlée et comportant l’administration de plusieurs autres traitements pharmacologiques, les résultats positifs observés pourraient ne pas être uniquement attribuables à la kétamine (Goldfine et al., 2023).
Ces trois études, regroupant 116 patients, indiquent qu’à la suite d’une perfusion de kétamine, aucun effet secondaire grave n’a été observé. Néanmoins, dans l’étude de Wong et al. (2015), un patient a présenté une complication liée à un surdosage. Et dans l’étude de Shah et al. (2018), deux patients ont présenté de l’hypertension. Dans l’ensemble, les trois études confirment une efficacité de la kétamine dans la réduction des symptômes de sevrage ainsi que dans la diminution du besoin en BZD.
Quelques années plus tard, la kétamine a été étudiée pour son potentiel dans le traitement du TUA. Au total, 3 études cliniques randomisées et contrôlées sont disponibles (Das et al., 2019 ; Dakwar et al., 2020 ; Grabski et al., 2022), ainsi qu’une étude rétrospective, par interviews, reprenant une cohorte de patients ayant participé à l’un de ces essais cliniques (Mollaahmetoglu et al., 2021), et une étude rétrospective observationnelle se basant sur des données issues de la pratique privée (Kolp et al., 2007).
L’étude de Kolp et al. (2007) se base sur des données issues d’anciennes observations de Krupitsky et al. (1992) chez des patients ayant été traités avec de la kétamine, en partie dans un cadre clinique privé mais majoritairement en externe. Le protocole utilisé comportait une période de sevrage d’environ 3 semaines, suivie d’un accompagnement psychothérapeutique (psychothérapie de groupe ou psychothérapie individuelle) d’une durée de 3 semaines au cours desquelles les volontaires recevaient une ou deux injections de kétamine. Le nombre total de cas étudiés s’élevait à 70, parmi lesquels 25 % à 70 % ont déclaré être encore abstinents 1 an après l’intervention. Les taux d’abstinence les plus élevés ont été retrouvés pour les groupes ayant reçu deux injections de kétamine couplées à de la psychothérapie individuelle. Relativement peu d’informations sont disponibles au sujet des doses de kétamine utilisées ou encore du protocole expérimental.
En 2019, Das et al. rapportent les résultats d’une étude clinique randomisée et contrôlée en simple aveugle dans laquelle 90 patients volontaires sont inclus avec un niveau de consommation d’alcool dit à risque (score supérieur à 8 au questionnaire AUDIT – Alcohol Use Disorders Identification Test). Les auteurs suggèrent que la kétamine, par le blocage des R-NMDA, est capable de déstabiliser la reconsolidation des mémoires de récompenses inadaptées (MRI). Dans la procédure MRI, un apprentissage conditionné liant les stimuli environnementaux à la consommation d’une drogue conduit au développement et au maintien d’une dépendance. La présentation de stimuli environnementaux, comme l’odeur ou le goût de l’alcool, entraîne le rappel de la mémoire associée à la consommation d’alcool. Ce mécanisme est dépendant des récepteurs glutamatergiques, notamment les R-NMDA (Goldfine et al., 2023). Afin de déstabiliser les MRI, les auteurs utilisent une procédure de rappel de la mémoire associée à l’alcool par le biais d’une présentation de stimuli conditionnés. Ils suggèrent que la kétamine administrée après le rappel de la mémoire conditionnée pourrait empêcher la reconsolidation de la MRI, et ainsi réduire la motivation pour la consommation d’alcool et donc promouvoir l’abstinence. Trois groupes sont constitués pour cette étude (Das et al., 2019). Deux groupes reçoivent la kétamine (0,35 mg/mL sur 30 minutes en intraveineux), après rappel ou non de la MRI, et le groupe placebo est perfusé avec une solution saline après rappel de la MRI. Seul le groupe ayant reçu la kétamine en complément de la thérapie par déstabilisation de la MRI montre une réduction significative du nombre de jours passés à consommer de l’alcool, ainsi qu’une baisse significative des propriétés « renforçantes » de l’alcool. Ainsi, la kétamine, lorsqu’elle est administrée après le rappel de la MRI, est capable d’interférer avec la reconsolidation de ces mémoires. De manière intéressante, les auteurs ont montré que la consommation d’alcool à 9 mois était similaire pour les trois groupes. Toutefois, le groupe ayant reçu de la kétamine couplée à la psychothérapie montrait une diminution significative et très rapide de la consommation d’alcool, alors que les deux autres groupes présentaient une cinétique de diminution plus lente (Das et al., 2019). Ainsi, cette étude suggère que la kétamine seule est aussi efficace pour réduire la consommation d’alcool que la kétamine couplée à la psychothérapie, mais que cette réponse intervient plus tôt dans cette dernière configuration. Plusieurs défauts limitent cependant la portée de cette étude : (i) des niveaux de consommation différents entre les groupes, (ii) un nombre de sujets relativement faible ainsi que (iii) l’absence d’un groupe témoin (psychothérapie seule) (Das et al., 2019).
La deuxième étude clinique de Dakwar et al. (2020) s’intéresse à l’efficacité de la kétamine en association avec une psychothérapie de renforcement de la motivation, encore appelée psychothérapie de pleine conscience (Motivational Enhancement Therapy – MET). Dans cette étude randomisée, contrôlée et en double aveugle, 40 sujets alcoolodépendants sont traités dans un cadre ambulatoire. La durée totale de l’intervention est de 5 semaines, au cours desquelles les patients bénéficient d’abord de 6 sessions de MET les deux premières semaines, puis d’autres sessions plus espacées les semaines suivantes. Durant la deuxième semaine, les patients reçoivent une perfusion intraveineuse de kétamine (0,71 mg/kg, N = 17) ou de midazolam (0,025 mg/kg N = 23 ; « placebo actif ») d’une durée de 50 minutes. Au bout des trois dernières semaines de suivi, 52,9 % (9/17) des patients traités avec la kétamine rapportent avoir arrêté de consommer de l’alcool, contre 30,9 % (9/22) pour le groupe témoin ayant reçu le midazolam (un patient de ce groupe ne s’est pas représenté au centre après avoir été traité). Les entretiens téléphoniques 6 mois après l’intervention indiquent que 75 % des patients traités avec la kétamine sont restés abstinents contre 25 % pour le groupe midazolam. Mais cette étude également présente quelques limites, notamment un nombre de patients relativement faible ainsi que l’impossibilité de contacter certains patients 6 mois après l’intervention (Dakwar et al., 2020). Les auteurs suggèrent qu’un suivi à plus long terme renforcerait l’intensité des résultats obtenus. Enfin, ils proposent que les expériences mystiques observées chez les patients lors de la perfusion de kétamine pourraient jouer un rôle dans la réduction de la consommation d’alcool induite par le psychédélique associé à la psychothérapie MET.
L’étude clinique la plus récente est celle de Grabski et al. (2022), qui s’intéresse à l’efficacité et la sécurité de l’utilisation de la kétamine, en complément d’une thérapie comportementale et cognitive (TCC), pour diminuer le risque de rechute et maintenir l’abstinence. Cette étude randomisée et contrôlée sur 6 semaines a été réalisée sur un groupe de 96 patients présentant un TUA modéré à sévère. Après leur admission, les patients sont séparés en quatre groupes destinés à recevoir 3 perfusions de solution saline ou de kétamine (0,8 g/kg par voie intraveineuse, sur 40 minutes) couplées avec soit une psychothérapie TCC axée sur le maintien de l’abstinence et la prévention de la rechute, soit une éducation aux effets de l’alcool. Les taux d’abstinence à 6 mois indiquent que 65,8 % des patients ayant reçu de la kétamine n’ont pas rechuté, contre 27 % pour les groupes témoins (Grabski et al., 2022). Le nombre de jours d’abstinence est plus élevé pour le groupe ayant reçu de la kétamine couplée à de la TCC, comparé au groupe ayant participé au protocole d’éducation, mais cette différence n’est pas statistiquement significative. Dans cette étude, seuls deux patients du groupe kétamine ont présenté des effets secondaires sévères, notamment une tachycardie et une hypertension. Etant la première à inclure un groupe témoin avec de la psychothérapie seule, cette étude permet d’évaluer spécifiquement l’efficacité de la kétamine seule ou en combinaison avec la psychothérapie. Une limite est soulignée par les auteurs qui suggèrent que l’utilisation d’un placebo actif, comme le midazolam, aurait été plus appropriée que le choix d’un placebo neutre, e.g. la solution saline, dans leur étude (Grabski et al., 2022). Pour les auteurs de cette étude, les propriétés antidépressives de la kétamine, objectivées par la diminution des symptômes de dépression, jouent un rôle dans l’évolution favorable du TUA (Grabski et al., 2022). D’ailleurs, une autre étude sur un nombre de patients très limité (N = 5) avait également montré un effet positif de la kétamine sur l’état dépressif associé au TUA (Yoon et al., 2019). Dans cette étude ouverte, 4 hommes et une femme volontaires, souffrant de dépression et présentant un TUA, ont reçu de la kétamine (0,5 mg/kg, par voie intraveineuse) ainsi que de la naltrexone (380 mg, par voie orale) une fois par semaine, durant 4 semaines. Les auteurs rapportent que 4 des 5 patients avaient diminué leur consommation d’alcool et que tous présentaient un score de dépression abaissé (évalué par une réduction sur l’échelle MADRS).
Les données issues de l’étude de Grabski et al. (2022) ont été analysées également par l’équipe de Mollaahmetoglu et al. (2021). Ces derniers ont conduit une analyse rétrospective par interviews de 11 patients entre 1 et 3 ans après qu’ils aient reçu les 3 injections de kétamine, et pu noter que 3 de ces patients (soit 27 %) étaient encore abstinents au moment de l’interview. De plus, l’ensemble des patients rapporte une amélioration de leur condition et une diminution à fois de la consommation d’alcool et de l’envie de consommer (Mollaahmetoglu et al., 2021).
Les résultats de ces différentes études cliniques ont permis une avancée dans l’utilisation à la fois efficace et sécure de la kétamine dans le cadre du TUA. Dans l’ensemble, ces études prometteuses indiquent que l’administration de kétamine conduit non seulement à une réduction des symptômes de sevrage et du craving pour l’alcool, mais aussi à une augmentation de la durée d’abstinence. Les études les plus anciennes attribuent un rôle majeur à la psychothérapie dans l’efficacité du traitement par la kétamine, et des données récentes semblent en faveur de cette hypothèse, en montrant qu’un accompagnement psychothérapeutique individuel donne de meilleurs résultats qu’un traitement pharmacologique seul ou associé à une thérapie de groupe. Actuellement de nouvelles études cliniques sont en cours, qui devraient éclaircir certains points clés de la thérapie par kétamine. Notamment l’étude d’Elias Dakwar (NCT04084860), qui évalue l’efficacité de la kétamine seule ou associée à la psychothérapie, en comparaison avec la psychothérapie seule, sur un nombre de participants supérieur à 100 (N = 120). D’autres études méritent également d’être citées, comme par exemple celles de Gihyun Yoon (NCT02461927, N = 65) et de Dale Terasaki (NCT04562779, N = 60), qui visent toutes deux à évaluer l’efficacité de la kétamine comparée à la naltrexone où à la combinaison de ces deux molécules pour prolonger la durée d’abstinence. Pour sa part, Gihyun Yoon réalise aussi une étude (NCT02461927) sur les effets antidépresseurs de la kétamine et leur impact possible sur l’évolution du TUA. Enfin, deux autres études en cours [Ismene Petrakis (NCT01551329, N = 20) ; Rodrigo Machado-Vieira (NCT03539887, N = 33)] évaluent également les propriétés antidépressives de la kétamine chez des patients présentant une comorbidité dépression et TUA. Les résultats de ces études complémentaires devraient permettre d’accroître les connaissances acquises ces dix dernières années sur l’utilisation de la kétamine dans le traitement du TUA. La kétamine étant d’ores et déjà approuvée pour le traitement de la dépression, une transition facilitée au traitement du TUA est envisageable au regard de la forte comorbidité existant entre ces deux pathologies.
Résumé des études cliniques concernant l’utilisation de la kétamine dans le cadre du traitement du TUA. Ce tableau a été réalisé par une analyse bibliographique de l’ensemble des sources primaires ainsi que de différentes revues traitant de l’utilisation clinique de la kétamine. Dans ce tableau sont présentés : le type d’étude (RCT : Étude clinique randomisée et contrôlée, AWS : Étude clinique sur le syndrome de sevrage, Ancienne, Autre), les références de l’étude clinique ou des articles cliniques rapportant les résultats, le nombre de participants, l’objectif de l’étude comme décrit par les auteurs, un résumé de l’intervention pharmacologique et psychothérapeutique, ainsi que les résultats majeurs de chacune des études. L’absence d’un groupe contrôle est signifiée par « Aucun » dans la colonne « Contrôle ». L’étude de Condi et al., (1972), mentionnée dans le texte, n’a pas été incluse dans ce tableau en raison d’un manque d’informations.
Études précliniques
Les résultats des études cliniques sur la kétamine dans le traitement du TUA sont aussi étayés par plusieurs études précliniques. Ces dernières ont évalué l’efficacité de la kétamine pour réduire la consommation d’alcool (n = 6) ou diminuer des symptômes de sevrage (n = 3), comme résumé dans le Tableau 2. Les études précliniques sont très utiles dans l’exploration des mécanismes d’action à l’origine des effets thérapeutiques de la kétamine.
Les modèles précliniques du TUA peuvent être classés en deux catégories : les modèles d’alcoolisation passive ou de consommation active. Dans un modèle d’alcoolisation passive, l’animal reçoit de l’alcool par administration forcée, ou encore, l’alcool est rendu disponible dans les cages d’hébergement de l’animal. Un modèle d’alcoolisation est dit actif lorsque l’animal doit accomplir une tâche pour obtenir de l’alcool, ce qui n’est le cas que pour les modèles d’administration opérante d’alcool. Parmi les modèles d’alcoolisation passive, les plus fréquemment utilisés sont : l’accès continu, l’accès intermittent en situation de choix alcool/eau (IA2BC), le « Drinking in the Dark » (DID), l’inhalation chronique de vapeurs d’alcool (CIE) et l’injection intrapéritonéale d’alcool. Ces différents modèles ont été validés par un grand nombre d’études et sont utilisés pour caractériser les diverses dimensions du TUA comme la perte de contrôle ou l’usage persistant en dépit des conséquences négatives (usage compulsif). Les trois études examinant l’effet de la kétamine sur le syndrome de sevrage utilisent des modèles d’exposition passive, notamment le CIE (Getachew & Tizabi, 2019 ; McGinnis et al., 2020), et l’IA2BC (Holleran et al., 2016). Concernant les six études évaluant l’efficacité de la kétamine sur la consommation d’alcool, cinq études utilisent des modèles d’exposition passive, notamment le DID (Ruda-Kucerova et al., 2018 ; Crowley et al., 2019 ; Ardinger et al., 2021) et l’IA2BC (Rezvani et al., 2017 ; Strong et al., 2019) tandis que la 6e utilise un modèle de consommation opérante (Sabino et al., 2013).
La première étude examinant les effets de la kétamine sur le syndrome de sevrage alcoolique a été menée par Holleran et al. (2016). Les chercheurs ont exposé des souris femelles C57BL6/J (N = 232) à l’alcool pendant trois semaines via le paradigme d’accès intermittent en double choix (biberon d’éthanol 10 % et biberon d’eau), suivi d’une période d’abstinence forcée déclenchant l’apparition de symptômes dépressifs, évalués par le test de suppression de la nourriture par la nouveauté (NFST). Les résultats ont montré que l’injection préalable de kétamine (3 mg/kg IP), mais pas de mémantine (20 mg/kg IP), un autre antagoniste des R-NMDA, supprime les perturbations induites par le sevrage (Holleran et al., 2016).
L’étude de Getachew & Tizabi (2019) s’intéresse également aux symptômes de type dépressif liés à l’exposition à l’alcool. Les chercheurs ont exposé des rats mâles Wistar (N = 40) à des vapeurs d’éthanol 4 h par jour pendant une semaine. Après chaque session d’inhalation, les rats ont reçu une injection de kétamine (2,5 mg/kg IP) ou de NBQX (5 mg/kg IP), un antagoniste des R-AMPA et -kaïnate, seuls ou en combinaison. Les symptômes de dépression liés au sevrage alcoolique ont été évalués à l’aide du test de nage forcée. Dans ce test, une durée d’immobilité augmentée est synonyme d’une résignation et donc d’un état de type dépressif. Les résultats ont montré que les injections de kétamine et de NBQX diminuent les symptômes de type dépressif, les animaux traités présentant un temps d’immobilité non significativement différent de celui de rats témoins, non alcoolisés. Mais, curieusement, l’administration combinée des deux molécules n’a eu aucun effet. Les chercheurs ont également réalisé des analyses post-mortem sur des échantillons de cerveaux, ce qui leur a permis de quantifier les niveaux de BDNF, une protéine qui participe à la plasticité synaptique, la croissance des neurones ainsi qu’au maintien de la plasticité cérébrale. Les résultats ont montré que le sevrage entraînait une diminution des niveaux de BDNF dans l’hippocampe, et que la kétamine et le NBQX avaient permis le retour aux niveaux de base. En revanche, la combinaison des deux molécules n’a eu aucun effet, indiquant une inhibition mutuelle de leurs actions. Ces résultats suggèrent que la diminution du comportement de type dépressif induite par la kétamine chez les animaux alcoolisés-sevrés est associée au rétablissement des taux de BDNF dans l’hippocampe (Getachew & Tizabi, 2019).
La dernière étude sur le syndrome de sevrage alcoolique a été menée par McGinnis et al. (2020). Ces auteurs se sont intéressés aux altérations de la plasticité synaptique induites par l’alcool dans deux structures cérébrales, l’amygdale basolatérale (BLA) et le cortex insulaire agranulaire (AIC), qui sont en connexion réciproque et toutes deux impliquées dans la régulation des émotions. Ils ont exposé des rats Sprague Dawley mâles et femelles (N = 104) à des vapeurs d’alcool pendant 12 h par jour, tous les jours, pendant 7 ou 10 jours. Le sevrage après 10 jours d’exposition aux vapeurs d’éthanol, mais pas après 7 jours, a entraîné une augmentation de la fonction des R-AMPA au niveau postsynaptique de la projection AIC vers BLA. De plus, les courants ioniques liés à l’activation des R-NMDA sont également augmentés au niveau de ces synapses après une exposition aux vapeurs d’alcool pendant 10 jours. Les résultats comportementaux ont montré un phénotype de type anxieux, en particulier dans le test du labyrinthe en croix surélevé. L’injection de kétamine (10 mg/kg IP) après la dernière session d’inhalation a supprimé les modifications fonctionnelles des R-AMPA et R-NMDA ainsi que l’augmentation de l’anxiété induites par le sevrage (McGinnis et al., 2020).
Dans l’ensemble, ces trois études précliniques indiquent que la kétamine, administrée à des doses sub-anesthésiques, peut diminuer les symptômes de types dépressif et anxieux induits par le sevrage alcoolique.
Sabino et al. (2013) ont été les premiers à évaluer les effets de la kétamine, comparée à la mémantine, sur la consommation active d’alcool chez des rats TSRL (N = 19) dits « alcoolo-préférants » (ayant une propension à préférer une boisson alcoolisée lorsqu’ils ont le choix de consommer aussi de l’eau). Les animaux ont d’abord été exposés à l’alcool dans une procédure d’IA2BC (solution d’éthanol 10 %) avant d’être entraînés à la tâche d’auto-administration opérante d’éthanol (10 %). Leur consommation d’éthanol a été évaluée lors de la dernière session opérante, 30 minutes après l’administration de kétamine (0–20 mg/kg IP) ou de mémantine (0–10 mg/kg IP). Les résultats ont montré que la kétamine et la mémantine réduisent la consommation d’alcool de manière dose-dépendante, mais des expériences supplémentaires ont révélé que la kétamine réduit également la consommation de saccharose. L’administration de rapamycine, un inhibiteur de la voie de signalisation mTOR, a inhibé les effets de la kétamine et de la mémantine sur la consommation d’alcool. Au total, cette étude indique que les deux antagonistes non compétitifs des R-NMDA présentent un intérêt thérapeutique dans le cadre de l’alcoolodépendance et que leurs effets sont relayés par la voie de signalisation mTOR (Sabino et al., 2013).
Pour leur part, Rezvani et al. (2017) ont évalué les effets de la kétamine sur la consommation et la préférence pour l’éthanol chez des rats « alcoolo-préférants » (N = 18) à l’aide du même paradigme d’IA2BC. Les résultats ont montré que l’injection sous-cutanée de doses croissantes de kétamine (5, 7,5, 10 mg/kg) 15 minutes avant l’exposition à l’éthanol réduit à la fois la consommation et la préférence pour l’éthanol de manière dose-dépendante. La réponse à la kétamine est plus importante chez les femelles, bien qu’elles aient initialement consommé moins d’éthanol que les mâles. Ces résultats reflètent les différences de sensibilité à l’alcool et de neurotransmission glutamatergique observées entre les sexes ce qui devrait inciter à entreprendre des études supplémentaires pour en élucider les mécanismes biologiques sous-jacents.
Dans l’étude de Ruda-Kucerova et al. (2018), les auteurs ont comparé les effets de la kétamine (5 et 10 mg/kg, IP) à ceux du NBQX (5 et 10 mg/kg, IP) administrés seuls ou en combinaison. Des rats mâles Wistar (N = 60) ont été exposés à l’alcool pendant 6 semaines en suivant la procédure du DID, puis ont reçu les traitements 20 minutes avant la dernière session de cette procédure. Chez les rats traités par les deux molécules, l’injection de NBQX précédait celle de kétamine de 5 minutes (Ruda-Kucerova et al., 2018). Les deux doses de kétamine et la plus faible dose de NBQX ont réduit significativement la consommation d’alcool indépendamment du sexe. En revanche, l’injection combinée de NBQX et de kétamine n’a eu aucun effet, suggérant que le NBQX bloque les effets de la kétamine sur la consommation d’alcool. Cependant, cette étude n’a pas montré de blocage de l’effet antidépresseur de la kétamine par le NBQX. Ces résultats préliminaires ont été partiellement confirmés dans une étude ultérieure (Getachew & Tizabi, 2019). Les différences observées dans le test de nage forcée ainsi que les différences d’effet de la kétamine et du NBQX dans l’étude de Ruda-Kucerova et al. (2018) comparée à celle de Getachew & Tizabi (2019) pourraient être en lien avec l’utilisation de durées d’alcoolisation distinctes dans ces deux études (6 versus 3 semaines, respectivement).
La recherche conduite par Crowley et al. (2019) a consisté à évaluer les effets de l’alcool sur les niveaux d’expression des R-AMPA et R-NMDA ainsi que sur l’activité de la voie de signalisation mTOR. Cinquante-trois souris C57BL6/J ont été exposées à l’alcool selon la procédure de DID pendant 4 semaines. Les résultats ont montré que l’exposition à l’alcool réduit l’expression des R-NMDA et R-AMPA dans le cortex prélimbique, en particulier chez les souris femelles. De plus, une diminution de la neurotransmission glutamatergique dans cette structure a été observée, indépendamment du sexe. Cependant, l’administration de kétamine à une dose sub-anesthésique (3 mg/kg IP), 12 h avant la dernière session de DID, réduit significativement la consommation d’éthanol chez les femelles mais pas chez les mâles (bien qu’une tendance à la diminution soit observée). Par ailleurs, ce traitement rétablit la transmission glutamatergique (au même niveau que chez les rats témoins naïfs) dans le cortex prélimbique chez les deux sexes, alors qu’une transmission synaptique physiologique normale ne s’observe après l’administration de kétamine que chez les femelles. Enfin, Crowley et al. (2019) rapportent que l’exposition à l’alcool entraîne une diminution de l’activité de la voie de signalisation mTOR, et que la kétamine corrige cet effet, comme attendu d’un rôle important de mTOR dans les propriétés thérapeutiques de la kétamine (voir aussi Sabino et al., 2013).
Dans une autre étude, menée par Strong et al. (2019), 104 rats Sprague Dawley ont été exposés à la procédure d’IA2BC (éthanol 20 %) pendant 10 semaines. Quatre semaines après le début de l’exposition, les rats ont été entraînés à réaliser une tâche opérante pour obtenir de la kétamine, à raison de 50 μL en intraveineux, par appui sur le levier dit « actif ». L’objectif principal de cette étude était d’évaluer l’impact de l’éthanol sur les effets renforçants de la kétamine (« potentiel d’abus »), et celui de la kétamine sur la consommation d’éthanol. Les résultats ont montré que la kétamine réduit la consommation d’éthanol chez les rats mâles « grands buveurs », mais augmente celle des femelles « faibles consommatrices ». Ainsi, la kétamine, administrée de manière répétée au cours d’une consommation d’éthanol concomitante, semble présenter un fort potentiel « d’abus » chez les femelles mais pas chez les mâles. Il est intéressant de noter que les auteurs ont également observé une augmentation du BDNF au niveau du noyau accumbens, mais chez les rats mâles uniquement (Strong et al., 2019).
L’avant-dernière étude préclinique des effets de la kétamine sur la consommation d’éthanol que nous avons analysée est celle de Ardinger et al. (2021). Ces auteurs ont utilisé des souris C57BL6/J sélectionnées pour leur forte alcoolo-préférence (« Highly Alcohol Preferring » cHAP, N = 28) pour examiner l’effet de la kétamine spécifiquement sur la consommation de type binge drinking, qui se caractérise par la consommation d’une grande quantité d’alcool en un temps très court. Dans ce travail, le binge drinking a été modélisé avec une procédure DID où l’éthanol n’était disponible que pendant deux heures par session. Après deux semaines de DID, les souris ont reçu de la kétamine à la dose de 3 ou 10 mg/kg IP, mais ce traitement n’a pas eu d’effet significatif sur la consommation d’éthanol. Les souris ont ensuite été réinjectées avec des doses plus élevées de kétamine (32 et 100 mg/kg). Seule la dose de 100 mg/kg a significativement réduit la consommation d’éthanol, mais seulement pendant la session de binge drinking juste après l’injection (Ardinger et al., 2021).
Enfin, pour conclure cette partie concernant les données précliniques, il convient de mentionner l’étude de Franco et al. (2020) qui a montré que l’exposition à la kétamine durant l’adolescence réduit la préférence de place conditionnée par l’éthanol chez des rats Sprague Dawley mâles mais pas chez des femelles.
Résumé des études précliniques concernant l’évaluation des effets de la kétamine sur la consommation d’alcool et les symptômes de sevrage alcoolique. Ce tableau a été réalisé à partir de l’analyse bibliographique de l’ensemble des sources primaires ainsi que de différentes revues traitant de l’utilisation préclinique de la kétamine. Dans ce tableau sont présentés : le type d’étude (évaluant la consommation, AWS : évaluant les symptômes de sevrage, Autre), la référence de l’article préclinique, l’objectif des expériences, l’espèce utilisée, le modèle d’alcoolisation, une description précise de l’intervention pharmacologique, le délai d’administration des différentes molécules, ainsi que le type de contrôle utilisé. La colonne des résultats résume les conclusions majeures des auteurs. m: mâles, f: femelles, PN: jour post-natal, NR: non renseigné.
Bilan des évaluations cliniques et précliniques de l’intérêt thérapeutique potentiel de la kétamine pour le traitement des pathologies liées à l’alcool
Ainsi, dans l’ensemble, les études précliniques démontrent l’intérêt de la kétamine pour réduire la consommation d’éthanol ainsi que les symptômes de sevrage. Ces effets semblent d’intensité différente selon le sexe, les femelles présentant des réponses généralement plus importantes au traitement par la kétamine (Rezvani et al., 2017 ; Crowley et al., 2019 ; Strong et al., 2019). Cette sensibilité accrue pourrait s’expliquer par les différences de métabolisme de l’éthanol (Thomasson, 1995), ou encore par les différences de neuroplasticité en lien avec les spécificités concernant la libération des hormones sexuelles chez les femelles versus les mâles (McEwen, 1999 ; Holzhauer et al., 2020). De plus, la kétamine est métabolisée de manière différente selon le sexe, les femmes présentant des taux plus élevés de DNHK et de HNK que les hommes (Highland et al., 2022). Récemment, des études menées sur l’humain ont également souligné un certain nombre de différences liées au sexe concernant le développement, l’installation dans le temps et le traitement du TUA. Les femmes avec un TUA sont plus susceptibles de souffrir de troubles de l’humeur et d’anxiété comorbides que les hommes. Elles présentent également une plus grande prévalence de dépression majeure, de dépression induite par une substance, de troubles anxieux et de syndrome de stress post-traumatique (PTSD), et ont davantage tendance à consommer de l’alcool lorsqu’elles sont confrontées à des émotions négatives (Holzhauer et al., 2020). En particulier, les femmes qui présentent à la fois un TUA et un PTSD sont bien plus susceptibles que les hommes de boire pour faire face à l’affect négatif. Dans ce contexte, une thérapie à base de kétamine pourrait être particulièrement bénéfique pour les femmes souffrant d’un TUA, étant donné leur vulnérabilité accrue aux affects négatifs pendant le sevrage et leur taux plus élevé de dépression/d’anxiété comorbides (Holzhauer et al., 2020).
L’ensemble de ces données reflète la nécessité d’études cliniques et précliniques supplémentaires pour examiner les différences liées au sexe dans le TUA et dans le potentiel thérapeutique de la kétamine vis-à-vis de cette pathologie. À l’avenir, les investigations devraient inclure des groupes de sujets plus nombreux afin d’étudier les différences interindividuelles ainsi que l’impact de diverses comorbidités liées au TUA sur les réponses au traitement par la kétamine. Une limite importante à considérer pour son utilisation à des fins thérapeutiques est son potentiel « d’abus » dû à ses propriétés renforçantes. La kétamine procurant du plaisir, il subsiste un risque quant à son administration en chronique. D’ailleurs Chen et al. (2014), à Taiwan, ont également montré que les femmes prenant régulièrement de la kétamine avaient une consommation d’alcool plus élevée. Dès lors, dans le cadre du développement d’un traitement pour le TUA, spécifiquement chez la femme, le potentiel d’abus de la kétamine devrait être pris en compte et faire l’objet d’études complémentaires.
Les R-NMDA sont la cible de la kétamine. L’activité et le nombre de ces récepteurs dans le noyau accumbens et d’autres structures sont augmentés par une consommation chronique d’alcool (Morisot & Ron 2017 ; Ezquerra-Romano et al., 2018 ; Renteria et al., 2018 ; McGinnis et al., 2020). La kétamine, en tant qu’antagoniste des R-NMDA, pourrait se substituer à l’alcool et réduire les symptômes de sevrage qui surviennent après l’arrêt de la consommation (Wong et al., 2015 ; Pizon et al., 2018 ; Shah et al., 2018). Les effets antidépresseurs de la kétamine, qui impliquent les R-AMPA et les R-NMDA (Figure 3), pourraient également contribuer à la réduction des affects négatifs qui surviennent pendant et après le sevrage (Holleran et al., 2016 ; Getachew & Tizabi, 2019 ; McGinnis et al., 2020). Des études ont notamment mis en avant l’implication de l’augmentation d’activité des R-AMPA dans les propriétés antidépressives de la kétamine (Tizabi et al., 2012). Ces effets pourraient être en partie relayés par le (2R-6R)-HNK (Yao et al., 2018), justifiant l’importance de l’étude spécifique des différents métabolites dans le traitement du TUA.
La Figure 3 rappelle que les effets de la kétamine au niveau des synapses glutamatergiques impliquent la voie de signalisation mTOR (Li et al., 2021 ; Sabino et al., 2013 ; Crowley et al., 2019) et la libération du BDNF (Zanos et al., 2016 ; Abdallah et al., 2018 ; Ruda-Kucerova et al., 2018). Des études ont montré que l’addiction à l’alcool se caractérise par une diminution des taux de BDNF chez l’humain et chez le rongeur, et que ces taux sont restaurés par la kétamine dans le modèle animal (Zanardini et al., 2011 ; Pandey, 2016 ; Getachew & Tizabi, 2019). Or, le BDNF, qui participe aux phénomènes de neuroplasticité et de neurogenèse, est également diminué dans le cadre de la dépression (Kavalali & Monteggia, 2012 ; Browne & Lucki, 2013 ; Castrén & Monteggia, 2021). Ainsi, une hypothèse concernant le mécanisme d’action thérapeutique de la kétamine dans le cadre du TUA stipule que, par ses propriétés antidépressives, la kétamine favorise la libération de BDNF et corrige les déficits de neurogenèse observés après la consommation chronique d’alcool (Zanardini et al., 2011 ; Corne & Mongeau, 2019 ; Aleksandrova & Phillips, 2021).
Des études précliniques suggèrent que l’augmentation de la libération du BDNF dans le striatum dorsolatéral réduit le comportement d’auto-administration d’alcool (Jeanblanc et al., 2009, 2014). Les mêmes auteurs ont suggéré un mécanisme d’action faisant intervenir une expression accrue des récepteurs D3 de la dopamine, induite par le BDNF, au niveau du striatum dorsal (Jeanblanc et al., 2006). Ces effets multiples de la kétamine pourraient donc contribuer à réduire la consommation d’alcool à la fois directement et indirectement au travers d’une diminution des affects négatifs et des symptômes dépressifs comorbides. Ainsi, la kétamine favoriserait l’abstinence en prévenant, au moins en partie, les rechutes potentiellement induites par l’état dépressif.
Trois études précliniques rapportent également une réduction de la consommation d’alcool chez le rat sous l’action de la mémantine, un autre antagoniste des R-NMDA qui n’est pas hallucinogène (Sabino et al., 2013 ; Jeanblanc et al., 2014 ; Alaux-Cantin et al., 2015). Toutefois, contrairement à la kétamine, la mémantine ne semble pas prévenir la rechute chez le rat « alcoolodépendant » (Alaux-Cantin et al., 2015), ce qui suggère un mécanisme spécifique à la kétamine, bien que la voie de signalisation mTOR-BDNF semble être impliquée dans les effets de ces deux antagonistes des R-NMDA (Jeanblanc et al., 2014). De fait, ces dernières années, plusieurs auteurs (Autry & Monteggia, 2012 ; Kohtala et al., 2019 ; Casarotto et al., 2021 ; Lin et al., 2021 ; Cannarozzo et al., 2023 ; Xu et al., 2022) ont mis en avant une action spécifique de la kétamine, et de son métabolite (2R-6R)-HNK, ainsi que d’antidépresseurs « classiques », au niveau du récepteur-tyrosine kinase TRKB du BDNF. En particulier, la kétamine et la (2R-6R)-HNK agiraient en tant que modulateurs allostériques positifs en se fixant au niveau du domaine transmembranaire du récepteur TRKB, ce qui entraînerait sa translocation et sa stabilisation au niveau de la membrane plasmique, le rendant accessible au BDNF (Casarotto et al., 2021). Cette séquence a aussi été observée dans des expériences de privation mono-oculaire qui ont montré que la kétamine et son métabolite (2R-6R)-HNK étaient capables de promouvoir la dissociation de TRKB et de PTPσ (un inhibiteur de la voie de signalisation TRKB), favorisant ainsi la neuroplasticité dépendante de TRKB et le shift de dominance oculaire (Cannarozzo et al., 2023).
Cette dernière décennie, les études de la connectivité fonctionnelle cérébrale par imagerie en résonance magnétique fonctionnelle font partie de celles qui ont probablement le plus contribué au renouveau de l’intérêt thérapeutique potentiel des psychédéliques. Des recherches sur le LSD et la psilocybine ont permis d’élaborer la théorie de l’entropie cérébrale (Carhart-Harris et al., 2014 ; Carhart-Harris, 2018). Selon cette théorie, les psychédéliques, en réduisant la connectivité fonctionnelle au sein de réseaux neuronaux hiérarchisés, notamment le « Réseau de Mode par Défaut » (RMD), augmentent la connectivité fonctionnelle des réseaux primitifs avec le reste du cerveau. Des structures de réception des messages sensoriels, telles que le cortex visuel, voient leur activité augmentée, objectivée par un flux sanguin accru dans ces structures (Carhart-Harris et al., 2012, 2014, 2016), ce qui donne lieu à des hallucinations. Parallèlement, des réseaux plus évolués, impliqués dans la conscience de soi, comme le RMD, réduisent leur action neuromodulatrice sur les réseaux sous-jacents (Carhart-Harris et al., 2016 ; Carhart-Harris & Friston, 2019). Ainsi, sous l’action de la psilocybine et du LSD, la diminution de la connectivité fonctionnelle entre le cortex préfrontal médian et le RMD, ainsi qu’entre le cortex rétrosplénial, une structure du RMD, et le parahippocampe, conduit à la dissolution de l’ego (Carhart-Harris et al., 2016), un phénomène corrélé significativement avec l’amélioration des symptômes dépressifs (Sheline et al., 2010). La réduction de la connectivité fonctionnelle dans le RMD observée avec les psychédéliques, mais également avec la kétamine, pourrait être un mode de traitement de divers troubles psychiatriques (Bonhomme et al., 2016 ; Kadriu et al., 2020). Tout comme la dépression, l’addiction est le résultat d’un « cerveau bloqué » dans un schéma de pensée particulièrement néfaste pour l’individu malade (Grant & Harford, 1995 ; Hasin et al., 2007). Les psychédéliques, ainsi que la kétamine, pourraient permettre une restructuration fonctionnelle de la connectivité cérébrale, modifiant ainsi les schémas de pensée des individus (Kvam et al., 2018 ; Carhart-Harris & Friston, 2019 ; Mertens & Preller, 2021 ; Mendes et al., 2022). Dans ce contexte, la psychothérapie joue également un rôle important, permettant aux patients traités de visualiser clairement l’objectif de la session psychédélique ou de kétamine, améliorant ainsi l’efficacité et la durée de l’effet du traitement pharmacologique (Kolp et al., 2007 ; Grabski et al., 2022). Clairement, la psychothérapie associée à la kétamine, en raison de ses effets sur la plasticité et la neurogenèse, présente des avantages majeurs (pour davantage d’informations voir la revue de Ezquerra-Romano et al., 2018). Dans cette configuration, la kétamine permettrait d’ouvrir une fenêtre thérapeutique pendant laquelle le patient serait apte à acquérir de nouveaux apprentissages, modifiant ainsi son comportement à long terme (Das et al., 2019).
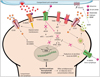 |
Figure 3 Schéma représentant le mécanisme d’action synaptique de la kétamine et de la 2R-6R-DHNK. L’activité neuronale pré-synaptique induit un relargage de glutamate au niveau du bouton synaptique. Le glutamate se fixe aux récepteurs-canaux AMPA et les rend perméables aux cations. L’entrée de charges positives entraîne une dépolarisation membranaire suffisamment élevée pour déclencher l’ouverture de canaux calciques voltage-dépendants (CCVD). Le calcium agit en tant que second messager et active la cascade de signalisation de la calmoduline kinase 2 ce qui a pour conséquence l’activation de la transcription CREB-dépendante. La fixation de la 2R-6R-DHNK au niveau des récepteurs AMPA déclenche leur activation, et donc l’entrée de Ca2+. La fixation de la kétamine dans le canal du récepteur NMDA inhibe son activité intracellulaire et empêche la phosphorylation de eEF2. p-eEF2 est un inhibiteur de CREB, ainsi la levée de cette inhibition favorise la synthèse protéique CREB-dépendante. L’activation de CREB entraîne la production locale de BDNF, et sa sécrétion est facilitée par le flux calcique entrant. Dans la fente synaptique, le BDNF agit sur le neurone pré-synaptique en augmentant la quantité de mGluR2 à sa surface. La kétamine et la 2R-6R-DHNK, en se fixant au domaine transmembranaire du récepteur TrkB du BDNF, facilitent sa présence à la surface. L’activation de TrkB permet la phosphorylation de GSK3β, et donc la levée de l’inhibition de mTORC1. L’inhibition des récepteurs NMDA extrasynaptiques entraîne également une levée de l’inhibition de mTORC1. Une fois actif, mTORC1 favorise la synthèse de protéines synaptiques, qui permettent la synaptogenèse et la neuroplasticité. L’ensemble de ces mécanismes est à l’origine des effets antidépresseurs de la kétamine ainsi que de la réduction de la consommation d’alcool. |
Conclusion
Des données convergentes suggèrent l’utilisation thérapeutique de la kétamine combinée ou non à une psychothérapie dans le traitement de l’addiction à l’alcool. Les études cliniques résumées plus haut (Tableau 1) sont unanimes quant à l’effet rapide de réduction de la consommation d’alcool et des taux de rechutes. La kétamine, qui présente relativement peu d’effets secondaires, est déjà disponible en tant qu’anesthésique et sous forme de spray pour le traitement de la dépression majeure, ce qui facilite son introduction en tant que traitement de l’addiction. Cependant, certaines limites sont aussi évidentes. Les différences de réponse à la kétamine et ses énantiomères et métabolites entre les sexes nécessitent une attention particulière, bien que cela ne semble pas affecter la prise en charge des patients. À l’avenir, des études précliniques devraient être mises en œuvre en vue d’évaluer les effets respectifs de chaque métabolite de la kétamine chez les mâles et les femelles. Par ailleurs, les effets thérapeutiques de la kétamine chez l’humain requérant des injections multiples, que ce soit dans le cadre de la dépression ou de l’addiction, il serait particulièrement judicieux d’évaluer les effets à court et à long terme d’un traitement avec des doses multiples de kétamine dans des modèles d’alcoolisation pertinents, notamment ceux produisant des symptômes addictifs (perte de contrôle, usage compulsif et état émotionnel négatif). L’avantage des investigations précliniques est qu’elles permettent l’étude des phénomènes neurobiologiques à la base des effets thérapeutiques de la kétamine. Une meilleure compréhension de ces mécanismes pourrait éventuellement conduire au développement de composés similaires à la kétamine, mais sans effets secondaires. En clinique, des études randomisées et contrôlées avec un placebo actif, comprenant un nombre suffisant de patients, devraient être une priorité afin de valider les résultats très encourageants déjà obtenus avec la kétamine dans le traitement du TUA.
Références
- Abdallah, C.G., Sanacora, G., Duman, R.S., Krystal, J.H. (2018). The neurobiology of depression, ketamine and rapid-acting antidepressants: Is it glutamate inhibition or activation? Pharmacol Ther, 190, 148-158. [CrossRef] [PubMed] [Google Scholar]
- Alaux-Cantin, S., Buttolo, R., Houchi, H., Jeanblanc, J., Naassila, M. (2015). Memantine reduces alcohol drinking but not relapse in alcohol-dependent rats. Addict Biol, 20, 890-901. [CrossRef] [PubMed] [Google Scholar]
- Aleksandrova, L.R., Phillips, A.G. (2021). Neuroplasticity as a convergent mechanism of ketamine and classical psychedelics. Trends Pharmacol Sci, 42, 929-942. [CrossRef] [PubMed] [Google Scholar]
- Ardinger, C.E., Winkler, G., Lapish, C.C., Grahame, N.J. (2021). Effect of ketamine on binge drinking patterns in Crossed High Alcohol-Preferring (CHAP) mice. Alcohol, 97, 31-39. [CrossRef] [PubMed] [Google Scholar]
- Autry, A.E., Monteggia, L.M. (2012). Brain-derived neurotrophic factor and neuropsychiatric disorders. Pharmacol Rev, 64, 238-258. [CrossRef] [PubMed] [Google Scholar]
- Autry, A.E., Adachi, M., Nosyreva, E., Na, E.S., Los, M.F., Cheng, P.-F., Ege T., Kavalali, E.T., Monteggia, L.M. (2011). NMDA receptor blockade at rest triggers rapid behavioural antidepressant responses. Nature, 475, 91-95. [CrossRef] [PubMed] [Google Scholar]
- Berman, R.M., Cappiello, A., Anand, A., Oren, D.A., Heninger, G.R., Charney, S., Krystal. J.H. (2000). Antidepressant effects of ketamine in depressed patients. Biol Psychiatry, 47, 351-354. [CrossRef] [PubMed] [Google Scholar]
- Bird, C.I., Nadav V., Modlin L., Rucker, J.J.H. (2021). Psilocybin and MDMA for the treatment of trauma-related psychopathology. Int Rev Psychiatry (Abingdon, England), 33, 229-249. [Google Scholar]
- Bonhomme, V., Vanhaudenhuyse, A., Demertzi, A., Bruno M.A., Jaque, O., Bahri, M.A., Plenevaux, A., Boly, M., Boveroux, P., Soddu, A., Brichant, J.F., Maquet, P., Laureys, S. (2016). Resting-state network-specific breakdown of functional connectivity during ketamine alteration of consciousness in volunteers. Anesthesiology 125, 873-888. [CrossRef] [PubMed] [Google Scholar]
- Browne, C.A., Lucki, I. (2013). Antidepressant effects of ketamine: Mechanisms underlying fast-acting novel antidepressants. Front Pharmacol, 4, 161. [CrossRef] [PubMed] [Google Scholar]
- Cameron, L.P., Tombari, R.J., Ju, L., Pell, A.J., Hurley, Z.Q., Ehinger, Y., Vargas, M.V., McCarroll, M.N., Taylor, J.C., Myers-Turnbull, D., Liu, T., Yaghoobi, B., Laskowski, L.J., Anderson, I.E., Zhang, G., Viswanathan, J., Brown, B.M., Tjia, M., Dunlap, L.E., Rabow, Z.T., Fiehn, O., Wulff, H., McCorvy, J.D., Lein, P.J., Kokel, D., Ron, D., Peters, J., Zuo, Y., Olson, D.E. (2021). A non-hallucinogenic psychedelic analogue with therapeutic potential. Nature, 589, 474-479. [CrossRef] [PubMed] [Google Scholar]
- Cannarozzo, C., Rubiolo, A., Casarotto, P., Castrén, E. (2023). Ketamine and its metabolite 2R,6R-hydroxynorketamine promote ocular dominance plasticity and release tropomyosin-related kinase B from inhibitory control without reducing perineuronal nets enwrapping parvalbumin interneurons. Eur J Neurosci, 57, 940-950. [CrossRef] [PubMed] [Google Scholar]
- Cao, D., Yu, J, Wang, H., Luo, Z., Liu, X., He, L., Qi, J., Fan, L., Tang, L., Chen, Z., Li, J, Cheng, J., Wang, S. (2022). Structure-based discovery of nonhallucinogenic psychedelic analogs. Science, 375, 403-411. [CrossRef] [PubMed] [Google Scholar]
- Carhart-Harris, R.L. (2018). The entropic brain – Revisited. Neuropharmacology, 142, 167-178. [CrossRef] [PubMed] [Google Scholar]
- Carhart-Harris, R.L., Friston K.J. (2019). REBUS and the anarchic brain: Toward a unified model of the brain action of psychedelics. E.L. Barker (Ed). Pharmacol Rev, 71, 316-344. [CrossRef] [PubMed] [Google Scholar]
- Carhart-Harris, R.L., Erritzoe, D., Williams, T., Stone, J.M., Reed, L.J., Colasanti, A., Tyacke, R.J., Leech, R., Malizia, A.L., Murphy, K., Hobden, P., Evans, J., Feilding, A., Wise, R.G., Nutt, D.J. (2012). Neural correlates of the psychedelic state as determined by FMRI studies with psilocybin. Proc Natl Acad Sci USA, 109, 2138-2143. [CrossRef] [PubMed] [Google Scholar]
- Carhart-Harris R.L., Leech R., Hellyer P.J., Shanahan M., Feilding A., Tagliazucchi E., Chialvo D.R., Nutt D. (2014). The entropic brain: A theory of conscious states informed by neuroimaging research with psychedelic drugs. Front Human Neurosci, 8, 20. [Google Scholar]
- Carhart-Harris, R.L., Muthukumaraswamy S., Roseman L., Kaelen M., Droog W., Murphy K., Tagliazucchi E., Schenberg, E.E., Nest, T., Orban, C., Leech, R., Williams, L.T., Williams, T.M., Bolstridge, M., Sessa, B., McGonigle, J., Sereno, M.I., Nichols, D., Hellyer, P.J., Hobden, P., Evans, J., Singh, K.D., Wise, R.G., Curran, H.V., Feilding, A., Nutt, D.J. (2016). Neural correlates of the LSD experience revealed by multimodal neuroimagin. Proc Natl Acd Sci USA, 113, 4853-4858. [CrossRef] [PubMed] [Google Scholar]
- Casarotto P.C., Girych, M., Fred, S.M., Kovaleva, V., Moliner, R., Enkavi, G., Biojone, C., Cannarozzo, C., Sahu, M.P., Kaurinkoski, K., Brunello, C.A., Steinzeig, A., Winkel, F., Patil, S., Vestring, S., Serchov, T., Diniz, C.R.A.F., Laukkanen, L., Cardon, I., Antila, H., Rog, T., Piepponen, T.P., Bramham, C.R., Normann, C., Lauri, S.E., Saarma, M., Vattulainen, I., Castrén, E. (2021). Antidepressant drugs act by directly binding to TRKB neurotrophin receptors. Cell, 184, 1299-1313. [CrossRef] [PubMed] [Google Scholar]
- Castrén, E, Monteggia, L.M. (2021). Brain-derived neurotrophic factor signaling in depression and antidepressant action. Biol Psychiatry, 90, 128-136. [CrossRef] [PubMed] [Google Scholar]
- Chen, W.Y., Huang M.C., Lin S.K. (2014). Gender differences in subjective discontinuation symptoms associated with ketamine use. Subst Abuse Treat Prev Policy, 9, 39. [CrossRef] [PubMed] [Google Scholar]
- Condi, M., Sallerin, T., Devaux, C. (1972). Use of ketamine in the treatment of delirium tremens and medical delirium. Anesthesie, Analgesie, Reanimation, 29, 377-394. [PubMed] [Google Scholar]
- Corne, R., Mongeau, R. (2019). Neurotrophic mechanisms of psychedelic therapy. Biologie Aujourd’hui, 213, 121-129. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Costa A.C., Joaquim H.P.G., Pedrazzi J.F.C., Pain A.O., Duque G., Aprahamian I. (2022). Cannabinoids in late life Parkinson’s disease and dementia: Biological pathways and clinical challenges. Brain Sci, 12, 1596. [CrossRef] [PubMed] [Google Scholar]
- Crowley, N.A., Magee, S.N., Feng, M., Jefferson, S.J., Morris, C.J., Dao, N.C., Brockway, D.F., Luscher, B. (2019). Ketamine normalizes binge drinking-induced defects in glutamatergic synaptic transmission and ethanol drinking behavior in female but not male mice. Neuropharmacology, 149, 35-44. [CrossRef] [PubMed] [Google Scholar]
- Dakwar, E., Anerella, C., Hart C.L, Levin F.R., Mathew S.J., Nunes, E.V. (2014). Therapeutic infusions of ketamine: Do the psychoactive effects matter? Drug Alcohol Depend, 136, 153-157. [CrossRef] [PubMed] [Google Scholar]
- Dakwar, E., Levin, F., Hart, C.L., Basaraba, C., Choi, J., Pavlicova, M., Nunes, E.V. (2020). A single ketamine infusion combined with motivational enhancement therapy for alcohol use disorder: A randomized midazolam-controlled pilot trial. Am J Psychiatry, 177, 125-133. [CrossRef] [PubMed] [Google Scholar]
- Das, R.K., Gale, G., Walsh, K., Hennessy, V.E., Iskandar, G., Mordecai, L.A., Brandner, B., Kindt, M., Curran, H.V., Kamboj, S.K. (2019). Ketamine can reduce harmful drinking by pharmacologically rewriting drinking memories. Nat Commun, 10, 5187. [CrossRef] [PubMed] [Google Scholar]
- De Gregorio, D., Aguilar-Valles, A., Preller, K.H., Heifets, B.D., Hibicke, M., Mitchell, J., Gobbi, G. (2021). Hallucinogens in mental health: Preclinical and clinical studies on LSD, Psilocybin, MDMA, and Ketamine. J Neurosci, 41, 891-900. [Google Scholar]
- DiazGranados, N., Ibrahim, L.A., Brutsche, N.E., Ameli, R., Henter, I.D., Luckenbaugh, D.A., Machado-Vieira, R., Zarate, C.A. Jr. (2010). Rapid resolution of suicidal ideation after a single infusion of an N-Methyl-D-Aspartate antagonist in patients with treatment-resistant major depressive disorder. J Clin Psychiatry, 71, 1605-1611. [CrossRef] [PubMed] [Google Scholar]
- Dworkin, R.H., Anderson, B.T., Andrews, N., Edwards, R.R., Grob, C.S., Ross, S., Satterthwaite, T.D., Strain, E.C. (2022). If the doors of perception were cleansed, would chronic pain be relieved? Evaluating the benefits and risks of psychedelics. J Pain, 23, 1666-1679. [CrossRef] [PubMed] [Google Scholar]
- Ebert, B., Mikkelsen, S., Thorkildsen C., Borgbjerg, F.M. (1999). Norketamine, the main metabolite of ketamine, is a non-competitive NMDA receptor antagonist in the rat cortex and spinal cord. Eur J Pharmacol, 333, 99-104. [Google Scholar]
- Ezquerra-Romano, I., Lawn, W., Krupitsky E., Morgan C.J.A. (2018). Ketamine for the treatment of addiction: Evidence and potential mechanisms. Neuropharmacology, 142, 72-82. [CrossRef] [PubMed] [Google Scholar]
- Feduccia, A.A., Mithoefer, M.C. (2018). MDMA-assisted psychotherapy for PTSD: Are memory reconsolidation and fear extinction underlying mechanisms? Prog Neuro-Psychopharmacol Biol Psychiatry, 84, 221-228. [CrossRef] [Google Scholar]
- Franco, D., Zamudio, J., Blevins, K.M., Núñez-Larios, E.A., Ricoy, U.M., Iñiguez, S.D., Zavala, A.R. (2020). Early-life ketamine exposure attenuates the preference for ethanol in adolescent Sprague Dawley rats. Behav Brain Res, 389, 112626. [CrossRef] [PubMed] [Google Scholar]
- Frohlich, J., Van Horn J.D. (2014). Reviewing the ketamine model for schizophrenia. J Psychopharmacol, 28, 287-302. [CrossRef] [PubMed] [Google Scholar]
- Garel, N., McAnulty, C., Greenway, K.T., Lesperance, P., Miron, J.P., Rej, S., Richard-Devantoy, S., Jutras-Aswad, D. (2022). Efficacy of ketamine intervention to decrease alcohol use, cravings, and withdrawal symptoms in adults with problematic alcohol use or alcohol use disorder: A systematic review and comprehensive analysis of mechanism of actions. Drug Alcohol Depend, 239, 109606. [CrossRef] [PubMed] [Google Scholar]
- Getachew, B., Tizabi, Y. (2019). Both ketamine and NBQX attenuate alcohol-withdrawal induced depression in male rats. J Drug Alcohol Res, 8, 236069. [PubMed] [Google Scholar]
- Goldfine C.E., Tom J.J., Im D.D., Yudkoff B., Anand A., Taylor J.J., Chai P.R., Suzuki J. (2023). The therapeutic use and efficacy of ketamine in alcohol use disorder and alcohol withdrawal syndrome: a scoping review. Front Psychiatry, 14, 11. [CrossRef] [Google Scholar]
- Grabski, M., Borissova, A., Marsh, B., Morgan C.J.A., Curran, H.V. (2020). Ketamine as a mental health treatment: Are acute psychoactive effects associated with outcomes? A Systematic Review. Behav Brain Res, 392, 112629. [CrossRef] [PubMed] [Google Scholar]
- Grabsk, M., McAndrew, A., Lawn, W., Marsh, B., Raymen, L., Stevens, T., Hardy, L., Warren, F., Bloomfield, M., Borissova, A., Maschauer, E., Broomby, R., Price, R., Coathup, R., Gilhooly, D., Palmer, E., Gordon-Williams, R., Hill, R., Harris, J., Mollaahmetoglu, O.M., Curran, H.V., Brandner, B., Lingford-Hughes, A., Morgan, C.J.A. (2022). Adjunctive ketamine with relapse prevention-based psychological therapy in the treatment of alcohol use disorder. Am J Psychiatry 179, 152-162. [CrossRef] [PubMed] [Google Scholar]
- Grant, B.F., Harford, T.C. (1995). Comorbidity between DSM-IV alcohol use disorders and major depression: Results of a national survey. Drug Alcohol Depend, 39, 197-206. [CrossRef] [MathSciNet] [Google Scholar]
- Hameed, M., Prasad, S., Jain, E., Dogrul, B.N., Al-Oleima, T.A., Pokhrel, B., Chowdhury, S., Co, E.L., Mitra, S., Quinonez, J., Ruxmohan, S., Stein, J. (2023). Medical cannabis for chronic nonmalignant pain management. Curr Pain Headache Rep, 27, 57-63. [CrossRef] [PubMed] [Google Scholar]
- Hasbi, A., Madras B.K., George S.R. (2023). Endocannabinoid system and exogenous cannabinoids in depression and anxiety: A review. Brain Sci, 13, 325. [CrossRef] [PubMed] [Google Scholar]
- Hasin, D.S., Stinson F.S., Ogburn E., Grant B.F. (2007). Prevalence, correlates, disability, and comorbidity of DSM-IV alcohol abuse and dependence in the United States: Results From the national epidemiologic survey on alcohol and related conditions. Arch Gen Psychiatry, 64, 830-842. [CrossRef] [PubMed] [Google Scholar]
- Heifets, B.D., Bentzley B.S, Williams N., Schatzberg A.F. (2021). Unraveling the opioid actions of S-Ketamine and R-Ketamine: Comment on Bonaventura et al. Mol Psychiatry, 26, 6104-6106. [CrossRef] [PubMed] [Google Scholar]
- Hess, E.M., Riggs, L.M., Michaelides, M., Gould T.D. (2022). Mechanisms of ketamine and its metabolites as antidepressants. Biochem Pharmacol, 197, 114892. [CrossRef] [PubMed] [Google Scholar]
- Highland J.N., Farmer, C.A., Zanos, P., Lovett, J., Zarate, C.A. Jr., Moaddel, R., Gould, T.D. (2022). Sex-dependent metabolism of ketamine and (2R,6R)-hydroxynorketamine in mice and humans. J Psychopharmacol, 36, 170-182. [CrossRef] [PubMed] [Google Scholar]
- Holleran K.M., Wilson H.H., Fetterly T.L., Bluett R.J., Centanni S.W., Gilfarb R.A., Rocco L.E., Patel S., Winder D.G. (2016). Ketamine and MAG lipase inhibitor-dependent reversal of evolving depressive-like behavior during forced abstinence from alcohol drinking. Neuropsychopharmacology, 41, 2062-2071. [CrossRef] [PubMed] [Google Scholar]
- Holzhauer, C.G., Cucciare, M., Epstein E.E. (2020). Sex and gender effects in recovery from alcohol use disorder. Alcohol Res, 40, 03. [CrossRef] [PubMed] [Google Scholar]
- Jeanblanc, J., He, D.Y., Mc, Gough, N.N., Logrip, M.L., Phamluong, K., Janak, P.H., Ron, D. (2006). The dopamine D3 receptor is part of a homeostatic pathway regulating ethanol consumption. J Neurosci, 26, 1457-1464. [CrossRef] [PubMed] [Google Scholar]
- Jeanblanc, J., He, D.Y., Carnicella, S., Kharazia, V., Janak, P.H., Ron, D. (2009). Endogenous BDNF in the dorsolateral striatum gates alcohol drinking. J Neurosci, 29, 13494-13502. [CrossRef] [PubMed] [Google Scholar]
- Jeanblanc, J., Coune, F. Botia, B., Naassila, M. (2014). Brain-derived neurotrophic factor mediates the suppression of alcohol self-administration by memantine. Addiction Biology, 19, 758-769. [CrossRef] [PubMed] [Google Scholar]
- Jelen, L.A., Young, A.H., Stone J.M. (2021). Ketamine: A tale of two enantiomers. J Psychopharmacol, 35, 109-123. [CrossRef] [PubMed] [Google Scholar]
- Joffe, M.E., Centanni, S.W., Jaramillo, A.A., Winder, D.G., Conn P.J. (2018). Metabotropic glutamate receptors in alcohol use disorder: Physiology, plasticity, and promising pharmacotherapies. ACS Chem Neurosci, 9, 2188-2204. [CrossRef] [PubMed] [Google Scholar]
- Kadriu, B., Greenwald, M., Henter, I.D., Gilbert, J.R., Kraus, C., Park, L.T., Zarate, C.A. (2020). Ketamine and serotonergic psychedelics: Common mechanisms underlying the effects of rapid-acting antidepressants. Int J Neuropsychopharmacol, 24, 8-21. [Google Scholar]
- Kavalali, E.T., Monteggia, L.M. (2012). Synaptic mechanisms underlying rapid antidepressant action of ketamine. Am J Psychiatry, 169, 1150-1156. [CrossRef] [PubMed] [Google Scholar]
- Klein, K., Zanger, U.M. (2013). Pharmacogenomics of cytochrome P450 3A4: Recent progress toward the “missing heritability” problem. Front Genetics, 4, 12. [CrossRef] [Google Scholar]
- Kohtala, S. (2021). Ketamine-50 years in use: From anesthesia to rapid antidepressant effects and neurobiological mechanisms. Pharmacol Rep, 73, 323-345. [CrossRef] [PubMed] [Google Scholar]
- Kohtala, S., Theilmann, W., Rosenholm, M., Müller, H.K., Kiuru, P., Wegener, G., Yli-Kauhaluoma, J., Rantamäki, T. (2019). Ketamine-induced regulation of TrkB-GSK3β signaling is accompanied by slow EEG oscillations and sedation but is independent of hydroxynorketamine metabolites. Neuropharmacology, 157, 107684. [CrossRef] [PubMed] [Google Scholar]
- Kokkinou, M., Ashok, A.H., Howes, O.D. (2018). The effects of ketamine on dopaminergic function: Meta-analysis and review of the implications for neuropsychiatric disorders. Mol Psychiatry, 23, 59-69. [CrossRef] [PubMed] [Google Scholar]
- Kolp, E., Young, S.A.M., Freidman, H., Krupitsky, E., Jansen, K., O’Connor, L-A. (2007). Ketamine-enhanced psychotherapy: Preliminary clinical observations on its effects in treating death anxiety. Int J Transpersonal Studies, 26, 1-17. [CrossRef] [Google Scholar]
- Krupitsky, E.M., Grinenko, A.Y. (1997). Ketamine Psychedelic Therapy (KPT): A review of the results of ten years of research. J Psychoact Drugs, 29, 165-183. [CrossRef] [PubMed] [Google Scholar]
- Krupitsky, E.M., Grinenko, A.Y., Berkaliev, T.N., Paley, A.I., Tetrov, U.N, Mushkov, K.A., Borodikin, Y.S. (1992). The combination of psychedelic and aversive approaches in alcoholism treatment: The affective contra-attribution method. Alcohol Treat Q, 9, 99-105. [CrossRef] [Google Scholar]
- Kvam, T.-M., Stewart, L.H., Andreassen, O.A. (2018). Psychedelic drugs in the treatment of anxiety, depression and addiction. Tidsskr Nor Legeforen, 138(18). doi.org/10.4045 [Google Scholar]
- Li, J., Areal, C.C., Toffa, D.H., Citherlet, D., Deacon, C., Jutras-Aswad, D., Keezer, M.R., Nguyen, D.K. (2023). Use of non-medical cannabis in epilepsy: A scoping review. Front Neurol, 14, 1132106. [CrossRef] [PubMed] [Google Scholar]
- Li, N., Lee, B., Liu, R.J., Banasr, M., Dwyer, J.M., Iwata, M., Li, X.Y., Aghajanian, G., Duman, R.S. (2021). mTOR-dependent synapse formation underlies the rapid antidepressant effects of NMDA antagonists. Science, 329, 959-964. [Google Scholar]
- Lin, P.Y., Ma, Z.Z., Mahgoub, M., Kavalali, E.T., Monteggia, L.M. (2021). A synaptic locus for TrkB signaling underlying ketamine rapid antidepressant action. Cell Rep, 36, 109513. [CrossRef] [PubMed] [Google Scholar]
- Lydic, R., Baghdoyan, H.A. (2002). Ketamine and MK-801 decrease acetylcholine release in the pontine reticular formation, slow breathing, and disrupt sleep. Sleep, 25, 617-622. [PubMed] [Google Scholar]
- McAndrew, A., Lawn, W., Stevens, T., Porffy, L., Brandner, B., Morgan, C.J. (2017) A proof-of-concept investigation into ketamine as a pharmacological treatment for alcohol dependence: study protocol for a randomised controlled trial. Trials, 18, 159. [CrossRef] [PubMed] [Google Scholar]
- McEwen, B.S. (1999). Permanence of brain sex differences and structural plasticity of the adult brain. Proc Nal Acad Sci USA, 96, 7128-7130. [CrossRef] [PubMed] [Google Scholar]
- McGinnis, M.M., Parrish, B.C., McCool, B.A. (2020). Withdrawal from chronic ethanol exposure increases postsynaptic glutamate function of insular cortex projections to the rat basolateral amygdala. Neuropharmacology, 172, 108129. [CrossRef] [PubMed] [Google Scholar]
- Meinhardt, M.W., Hansson, A.C., Perreau-Lenz, S., Bauder-Wenz, C., Stählin, O., Heilig, M., Harper, C., Drescher, K.U., Spanagel, R., Sommer, W.H. (2013). Rescue of infralimbic MGluR2 deficit restores control over drug-seeking behavior in alcohol dependence. J Neurosci, 33, 2794-2806. [CrossRef] [PubMed] [Google Scholar]
- Meinhardt, M.W., Pfarr, S., Fouquet, G., Rohleder, C., Meinhardt, M., Barroso-Flores, J., Hoffmann, R., Jeanblanc, J., Paul, E., Wagner, K., Hansson, A.C., Köhr, G., Meier, N., von Bohlen und Halbach, O., Bell, R.L., Endepols, H., Neumaier, B., Schönig, K., Bartsch, D., Naassila, M., Spanagel, R., Sommer, W.H. (2021). Psilocybin targets a common molecular mechanism for cognitive impairment and increased craving in alcoholism. Sci Adv, 7, eabh2399. [CrossRef] [PubMed] [Google Scholar]
- Mendes, F.R., dos Santos Costa, C., Wiltenburg, V.D., Morales-Lima, G., Fernandes, J.A.B., Filev, R. (2022). Classic and non-classic psychedelics for substance use disorder: A review of their historic, past and current research. Addiction Neurosci, 3, 100025. [CrossRef] [Google Scholar]
- Mertens, L.J., Preller K.H. (2021). Classical psychedelics as therapeutics in psychiatry – Current clinical evidence and potential therapeutic mechanisms in substance use and mood disorders. Pharmacopsychiatry, 54, 176-190. [CrossRef] [PubMed] [Google Scholar]
- Modaresi, F., Talachian, K. (2022). The characteristics of clinical trials on cannabis and cannabinoids: A review of trials for therapeutic or drug development purposes. Pharmaceutical Med, 36, 387-400. [CrossRef] [PubMed] [Google Scholar]
- Mollaahmetoglu, O.M., Keeler, J., Ashbullby, K.J., Ketzitzidou-Argyri, E., Grabski M., Morgan C.J.A. (2021). “This is something that changed my life”: A qualitative study of patients experiences in a clinical trial of ketamine treatment for alcohol use disorders. Front Psychiatry, 12, 695335. [CrossRef] [PubMed] [Google Scholar]
- Moreno, J.L., Holloway, T., Albizu, L., Sealfon, S.C., González-Maeso, J. (2011). Metabotropic glutamate MGlu2 receptor is necessary for the pharmacological and behavioral effects induced by hallucinogenic 5-HT2A receptor agonists. Neurosci Lett, 493, 76-79. [CrossRef] [PubMed] [Google Scholar]
- Morgan, C.J.A., Curran, H.V., Independent Scientific Committee on Drugs. (2012). Ketamine use: A review. Addiction, 107, 27-38. [CrossRef] [PubMed] [Google Scholar]
- Morisot, N., Ron, D. (2017). Alcohol-dependent molecular adaptations of the NMDA receptor system. Genes, Brain, Behav, 16, 139-148. [CrossRef] [PubMed] [Google Scholar]
- Olson, D.E. (2021). The subjective effects of psychedelics may not be necessary for their enduring therapeutic effects. ACS Pharmacol Transl Sci, 4, 563-567. [CrossRef] [PubMed] [Google Scholar]
- Orhurhu, V., Orhurhu, M.S., Bhatia, A., Cohen S.P. (2019). Ketamine infusions for chronic pain: A systematic review and meta-analysis of randomized controlled trials. Anesth Analg, 129, 241-254. [CrossRef] [PubMed] [Google Scholar]
- Orsolini, L., Chiappini, S., Volpe, U., De Berardis, D., Latini, R., Papanti, G.D., Corkery, A.J.M. (2019). Use of medicinal cannabis and synthetic cannabinoids in post-traumatic stress disorder (PTSD): A systematic review. Medicina (Kaunas, Lithuania), 55, 525. [CrossRef] [PubMed] [Google Scholar]
- Pandey, S.C. (2016). A critical role of brain-derived neurotrophic factor in alcohol consumption. Biol Psychiatry, 79, 427-429. [CrossRef] [PubMed] [Google Scholar]
- Peltoniemi, M.A., Hagelberg, N.M., Olkkola, K.T., Saari T.I. (2016). Ketamine: A review of clinical pharmacokinetics and pharmacodynamics in anesthesia and pain therapy. Clin Pharmacokin, 55, 1059-1077. [CrossRef] [PubMed] [Google Scholar]
- Pizon, A.F., Lynch, M.J., Benedict, N.J., Yanta, J.H., Frisch, A., Menke, N.B., Swartzentruber, G.S., King, A.M., Abesamis, M.G., Kane-Gill, S.L. (2018). Adjunct ketamine use in the management of severe ethanol withdrawal. Critical Care Medicine, 46, e 768-771. [Google Scholar]
- Renteria, R., Baltz, E.T., Gremel C.M. (2018). Chronic alcohol exposure disrupts top-down control over basal ganglia action selection to produce habits. Nat Commun, 9, 211. [CrossRef] [PubMed] [Google Scholar]
- Rezvani, A. H., Levin, E. D., Cauley, M., Getachew, B., Tizabi, Y. (2017). Ketamine differentially attenuates alcohol intake in male versus female alcohol preferring (P) rats. J Drug Alcohol Res, 6, 236030. [CrossRef] [Google Scholar]
- Rothberg, R.L., Azhari, N., Haug, N.A. Dakwar, E. (2021). Mystical-type experiences occasioned by ketamine mediate its impact on at-risk drinking: results from a randomized, controlled trial. J Psychopharmacol, 35, 150-158. [CrossRef] [PubMed] [Google Scholar]
- Ruda-Kucerova, J., Babinska, Z., Luptak, M., Getachew, B., Tizabi, Y. (2018). Both ketamine and NBQX attenuate alcohol drinking in male wistar rats. Neurosci Lett, 666, 175-180. [CrossRef] [PubMed] [Google Scholar]
- Sabino, V., Narayan, A.R., Zeric, T., Steardo, L., Cottone, P. (2013). mTOR activation is required for the anti-alcohol effect of ketamine, but not memantine, in alcohol-preferring rats. Behav Brain Res, 247, 9-16. [CrossRef] [PubMed] [Google Scholar]
- Saland, S.K., Kabbaj, M. (2018). Sex differences in the pharmacokinetics of low-dose ketamine in plasma and brain of male and female rats. J Pharmacol Exp Ther, 367, 393-404. [CrossRef] [PubMed] [Google Scholar]
- Sanders, B., Brula, A.Q. (2021). Intranasal esketamine: From origins to future implications in treatment-resistant depression. J Psychiatr Res, 137, 29-35. [CrossRef] [PubMed] [Google Scholar]
- Scotton, E., Antqueviezc, B., Vasconcelos, M.F., Dalpiaz, G., Paul Géa, L., Ferraz Goularte, J., Colombo, R., Ribeiro Rosa, A. (2022). Is (R)-Ketamine a potential therapeutic agent for treatment-resistant depression with less detrimental side effects? A review of molecular mechanisms underlying ketamine and its enantiomers. Biochem Pharmacol, 198, 114963. [CrossRef] [PubMed] [Google Scholar]
- Shah, P., McDowell, M., Ebisu, R., Hanif, T., Toerne, T. (2018). Adjunctive use of ketamine for benzodiazepine-resistant severe alcohol withdrawal: A retrospective evaluation. J Med Toxicol, 14, 229-236. [CrossRef] [PubMed] [Google Scholar]
- Sheline, Y. I., Price, J. L., Yan, Z., Mintun M. A. (2010). Resting-state functional MRI in depression unmasks increased connectivity between networks via the dorsal nexus. Proc Natl Acad Sci USA, 107, 11020-11025. [CrossRef] [PubMed] [Google Scholar]
- Shim, I. (2022). Distinct functions of S-Ketamine and R-Ketamine in mediating biobehavioral processes of drug dependency: Comments on Bonaventura et al. Mol Psychiatry. https://doi.org/10.1038/s41380-022-01629-0.20. [PubMed] [Google Scholar]
- Silvestre, J.S., Pallarés, M., Nadal, R., Ferré, N. (2002) Opposite effects of ethanol and ketamine in the elevated plus-maze test in Wistar rats undergoing a chronic oral voluntary consumption procedure. J Psychopharmacol, 16, 305-312. [CrossRef] [PubMed] [Google Scholar]
- Sos, P., Klirova, M., Novak, T., Kohutova, B., Horacek, J., Palenicek T. (2013). Relationship of ketamine’s antidepressant and psychotomimetic effects in unipolar depression. Neuro Endocrinol Lett, 34, 287-293. [PubMed] [Google Scholar]
- Strong, C.E., Kabbaj, M. (2020). Neural mechanisms underlying the rewarding and therapeutic effects of ketamine as a treatment for alcohol use disorder. Front Behav Neurosci, 14, 593860. [CrossRef] [PubMed] [Google Scholar]
- Strong, C.E., Wright, K.N., Kabbaj, M. (2019). Sex and individual differences in alcohol intake are associated with differences in ketamine self-administration behaviors and nucleus accumbens dendritic spine density. ENeuro 6(6): ENEURO.0221-19.2019. [CrossRef] [PubMed] [Google Scholar]
- Thomasson, H.R. (1995). Gender differences in alcohol metabolism. Physiological responses to ethanol. Recent Developments in Alcoholism, 12, 163-179. [PubMed] [Google Scholar]
- Tizabi, Y., Bhatti, B.H., Manaye, K.F, Das, J.R., Akinfiresoye, L. (2012). Antidepressant-like effects of low ketamine dose is associated with increased Hippocampal AMPA/NMDA receptor density ratio in female wistar-kyoto rats. Neuroscience, 213, 72-80. [CrossRef] [PubMed] [Google Scholar]
- Walsh, Z., Mollaahmetoglu, O.M., Rootman, J., Golsof, S., Keeler, J., Marsh, B., Nutt, D.J., Morgan, C.J.A. (2021). Ketamine for the treatment of mental health and substance use disorders: Comprehensive systematic review. BJPsych Open, 8, e19. [Google Scholar]
- Wei, Y., Chang, L., Hashimoto, K. (2020). A historical review of antidepressant effects of ketamine and its enantiomers. Pharmacol Biochem Behav, 190, 172870. [CrossRef] [PubMed] [Google Scholar]
- Williams, N.R., Heifets, B.D., Blasey, C., Sudheimer, K., Pannu, J., Pankow, H., Hawkins, J., Birnbaum, J., Lyons, D.M., Rodriguez, C.I., Schatzberg, A.F. (2018). Opioid receptor antagonism attenuates antidepressant effects of ketamine. Am J Psychiatry 175, 1205-1215. [CrossRef] [PubMed] [Google Scholar]
- Wong, A., Benedict, N.J, Armahizer, M.J., Kane-Gill, S.L. (2015). Evaluation of adjunctive ketamine to benzodiazepines for management of alcohol withdrawal syndrome. Ann Pharmacother, 49, 14-19. [CrossRef] [PubMed] [Google Scholar]
- Worrell, S. D., Gould, T.J. (2021). Therapeutic potential of ketamine for alcohol use disorder. Neurosci Biobehav Rev, 126, 573-589. [CrossRef] [PubMed] [Google Scholar]
- Xu, S., Yao, X., Li, B., Cui, R., Zhu, C., Wang, Y., Yang, W. (2022). Uncovering the underlying mechanisms of ketamine as a novel antidepressant. Front Pharmacol, 12, 740996. [CrossRef] [PubMed] [Google Scholar]
- Yaden, D.B., Griffiths R.R. (2021). The subjective effects of psychedelics are necessary for their enduring therapeutic effects. ACS Pharmacol Transl Sci, 4, 568-572. [CrossRef] [PubMed] [Google Scholar]
- Yao, N., Skiteva, O., Zhang, X., Svenningsson, P., Chergui K. (2018). Ketamine and its metabolite (2R,6R)-hydroxynorketamine induce lasting alterations in glutamatergic synaptic plasticity in the mesolimbic circuit. Mol Psychiatry, 23, 2066-2077. [CrossRef] [PubMed] [Google Scholar]
- Yoon, G., Petrakis, I.L., Krystal, J.H. (2019) Association of combined naltrexone and ketamine with depressive symptoms in a case series of patients with depression and alcohol use disorder. JAMA Psychiatry, 76, 337-338. [CrossRef] [PubMed] [Google Scholar]
- Zanardini, R., Fontana, A., Pagano, R., Mazzaro, E., Bergamasco, F., Romagnosi, G., Gennarelli, M., Bocchio-Chiavetto, L. (2011). Alterations of brain-derived neurotrophic factor serum levels in patients with alcohol dependence. Alcohol Clin Exp Res, 35, 1529-1533. [PubMed] [Google Scholar]
- Zanos, P., Moaddel, R., Morris, P.J., Georgiou, P., Fischell, J., Elmer, G.I., Alkondon, M., Yuan, P., Pribut H.J., Singh, N.S., Dossou, K.S., Fang Y., Huang X.P., Mayo, C.L., Wainer, I.W., Albuquerque, E.X., Thompson, S.M., Thomas, C.J., Zarate, C.A. Jr., Gould, T.D. (2016). NMDAR inhibition-independent antidepressant actions of ketamine metabolites. Nature, 533, 481-486. [CrossRef] [PubMed] [Google Scholar]
- Zanos, P., Highland, J.N., Stewart, B.W., Georgiou, P., Jenne, C.E., Lovett, J, Morris, P.J., Thomas, C.J., Moaddel, R., Zarate, C.A. Jr., Gould, T.D. (2019). (2R,6R)-Hydroxynorketamine exerts MGlu2 receptor-dependent antidepressant actions. Proc Natl Acad Sci USA, 116, 6441-6450. [CrossRef] [PubMed] [Google Scholar]
- Zarate, C.A. Jr., Brutsche, N., Laje, G., Luckenbaugh, D.A., Venkata, S.L., Ramamoorthy, A., Moaddel, R., Wainer, I.W. (2012). Relationship of ketamine’s plasma metabolites with response, diagnosis, and side effects in major depression. Biol Psychiatry, 72, 331-338. [CrossRef] [MathSciNet] [PubMed] [Google Scholar]
Citation de l’article : Hilal, F., Jeanblanc, J., et Naassila, M. (2023). Intérêt et mécanismes d’action de la kétamine dans le traitement de l’addiction à l’alcool – Revue des études cliniques et précliniques. Biologie Aujourd’hui, 217, 161-182
Liste des tableaux
Résumé des études cliniques concernant l’utilisation de la kétamine dans le cadre du traitement du TUA. Ce tableau a été réalisé par une analyse bibliographique de l’ensemble des sources primaires ainsi que de différentes revues traitant de l’utilisation clinique de la kétamine. Dans ce tableau sont présentés : le type d’étude (RCT : Étude clinique randomisée et contrôlée, AWS : Étude clinique sur le syndrome de sevrage, Ancienne, Autre), les références de l’étude clinique ou des articles cliniques rapportant les résultats, le nombre de participants, l’objectif de l’étude comme décrit par les auteurs, un résumé de l’intervention pharmacologique et psychothérapeutique, ainsi que les résultats majeurs de chacune des études. L’absence d’un groupe contrôle est signifiée par « Aucun » dans la colonne « Contrôle ». L’étude de Condi et al., (1972), mentionnée dans le texte, n’a pas été incluse dans ce tableau en raison d’un manque d’informations.
Résumé des études précliniques concernant l’évaluation des effets de la kétamine sur la consommation d’alcool et les symptômes de sevrage alcoolique. Ce tableau a été réalisé à partir de l’analyse bibliographique de l’ensemble des sources primaires ainsi que de différentes revues traitant de l’utilisation préclinique de la kétamine. Dans ce tableau sont présentés : le type d’étude (évaluant la consommation, AWS : évaluant les symptômes de sevrage, Autre), la référence de l’article préclinique, l’objectif des expériences, l’espèce utilisée, le modèle d’alcoolisation, une description précise de l’intervention pharmacologique, le délai d’administration des différentes molécules, ainsi que le type de contrôle utilisé. La colonne des résultats résume les conclusions majeures des auteurs. m: mâles, f: femelles, PN: jour post-natal, NR: non renseigné.
Liste des figures
 |
Figure 1 Les deux énantiomères de la kétamine. Ces deux énantiomères se différencient par leur conformation spatiale caractérisée par le carbone asymétrique noté 2 et conférant des propriétés physico-chimiques uniques à chaque énantiomère. Le groupement méthylamine NH-CH3 est dans le plan avant pour la R-kétamine et dans le plan arrière pour la S-kétamine. |
| Dans le texte | |
 |
Figure 2 La kétamine et les principaux métabolites de ses énantiomères. La S-kétamine et la R-kétamine sont d’abord métabolisées respectivement en S-norkétamine ou en R-norkétamine par les cytochromes P450. Ces deux premiers métabolites peuvent être métabolisés de nouveau pour donner la S-déhydronorkétamine (S-DHNK) ou la R-déhydronorkétamine (R-DHNK). Parallèlement la S-kétamine et la R-kétamine peuvent aussi être hydroxylées en S-hydroxykétamine (2S-6S-HK) et R-hydroxykétamine (2R-6R-HK) via le cytochrome PA6 puis ensuite métabolisées en 2S-6S-hydroxynorkétamine (2S-6S-HNK) et en 2R-6R-hydroxynorkétamine (2R-6R-HNK). |
| Dans le texte | |
 |
Figure 3 Schéma représentant le mécanisme d’action synaptique de la kétamine et de la 2R-6R-DHNK. L’activité neuronale pré-synaptique induit un relargage de glutamate au niveau du bouton synaptique. Le glutamate se fixe aux récepteurs-canaux AMPA et les rend perméables aux cations. L’entrée de charges positives entraîne une dépolarisation membranaire suffisamment élevée pour déclencher l’ouverture de canaux calciques voltage-dépendants (CCVD). Le calcium agit en tant que second messager et active la cascade de signalisation de la calmoduline kinase 2 ce qui a pour conséquence l’activation de la transcription CREB-dépendante. La fixation de la 2R-6R-DHNK au niveau des récepteurs AMPA déclenche leur activation, et donc l’entrée de Ca2+. La fixation de la kétamine dans le canal du récepteur NMDA inhibe son activité intracellulaire et empêche la phosphorylation de eEF2. p-eEF2 est un inhibiteur de CREB, ainsi la levée de cette inhibition favorise la synthèse protéique CREB-dépendante. L’activation de CREB entraîne la production locale de BDNF, et sa sécrétion est facilitée par le flux calcique entrant. Dans la fente synaptique, le BDNF agit sur le neurone pré-synaptique en augmentant la quantité de mGluR2 à sa surface. La kétamine et la 2R-6R-DHNK, en se fixant au domaine transmembranaire du récepteur TrkB du BDNF, facilitent sa présence à la surface. L’activation de TrkB permet la phosphorylation de GSK3β, et donc la levée de l’inhibition de mTORC1. L’inhibition des récepteurs NMDA extrasynaptiques entraîne également une levée de l’inhibition de mTORC1. Une fois actif, mTORC1 favorise la synthèse de protéines synaptiques, qui permettent la synaptogenèse et la neuroplasticité. L’ensemble de ces mécanismes est à l’origine des effets antidépresseurs de la kétamine ainsi que de la réduction de la consommation d’alcool. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.


